RESUMEN
ANTECEDENTES: El tumor de células de la granulosa es la neoplasia estromal de los cordones sexuales más común. La incidencia varía de 0.47 a 1.6 por cada 100,000 pacientes. Representa del 2 al 5% de todos los cánceres de ovario y se divide en dos subtipos, alrededor del 95% de los casos pertenecen a la estirpe adulta, y el resto a la estirpe juvenil. OBJETIVO: Exponer un caso de abdomen agudo con torsión de tumor ovárico, con desenlace favorable. Se realiza la revisión del tema para ampliar el conocimiento de la neoplasia.
CASO CLÍNICO: Paciente de 29 años, quien solicitó valoración ginecológica urgente por un cuadro de dolor abdominal generalizado, acentuado en la fosa iliaca izquierda, con distensión abdominal, timpanismo y peristalsis abolida. La exploración física y ultrasonográfica sugirió una tumoración compleja, dependiente de los anexos izquierdos, con probable torsión. Se decidió efectuar laparotomía exploratora de urgencia, con hallazgo transoperatorio de tumor ovárico izquierdo torsionado. El reporte anatomopatológico informó: tumor de células de la granulosa de estirpe juvenil torsionado. Los estudios de extensión resultaron negativos.
CONCLUSIÓN: Los tumores derivados de las células de la granulosa son excepcionales. La mayoría de los casos se diagnostican en etapas tempranas. La cirugía para estadificación, con estudio anatomopatológico transquirúrgico, es el tratamiento de referencia. La investigación futura debe centrarse en la exploración de los mecanismos moleculares del tumor de células de la granulosa y el desarrollo de medicamentos específicos.
PALABRAS CLAVE: Tumor de células de la granulosa, tumor de ovario, torsión tumoral, dolor abdomina, laparotomía exploradora, estadificación tumoral
ABSTRACT
BACKGROUND: Granulosa cell tumor is the most common stromal neoplasm of the sex cords. The incidence varies from 0.47 to 1.6 per 100,000 patients. It represents 2 to 5% of all ovarian cancers and is divided into two subtypes, around 95% of cases belong to the adult lineage, and the rest to the juvenile lineage.
CLINICAL CASE: 29-year-old patient, who requested urgent gynecological evaluation due to generalized abdominal pain, accentuated in the left iliac fossa, with abdominal distension, tympanism and abolished peristalsis. Physical and ultrasound examination suggested a complex tumor, dependent on the left adnexa, with probable torsion. It was decided to perform an emergency exploratory laparotomy, with transoperative finding of a torsed left ovarian tumor. The anatomopathological report informed: torsed juvenile lineage granulosa cell tumor. Extension studies were negative.
CONCLUSION: Tumors derived from granulosa cells are exceptional. Most cases are diagnosed at an early stage. Staging surgery with trans-surgical anatomopathological study is the reference treatment. Future research should focus on exploring the molecular mechanisms of granulosa cell tumor and developing specific drugs.
KEYWORDS: Granulosa cell tumor, ovarian tumor, tumor torsion, abdominal pain, exploratory laparotomy, tumor staging
ANTECEDENTES
El tumor de células de la granulosa es la neoplasia estromal de los cordones sexuales más común derivado de estas células.1 La incidencia varía de 0.47 a 1.6 por cada 100,000 pacientes. Representa del 2 al 5% de todos los tumores de ovario y se divide en dos subtipos, según la edad de las pacientes, características clínicas e histopatológicas.2 El 95% de los tumores de células de la granulosa pertenecen a la estirpe adulta y el resto a la estirpe juvenil.1 Los primeros aparecen solo en mujeres en edad reproductiva, con características de hiperestrogenismo y masa abdominal anormal.3 En general, los tumores de células de la granulosa son excepcionales, los tumores de estirpe adulta son frecuentes en mujeres de 50 a 55 años y los de estirpe juvenil en pacientes de 20 a 30 años.4 Las manifestaciones clínicas dependen de la edad de las pacientes. El tumor de células de la granulosa de estirpe adulta genera síntomas típicos de sangrado posmenopáusico y el de estirpe juvenil provoca síntomas relacionados con pubertad precoz.4 El tumor de células de la granulosa de la mujer adulta sugiere un tumor de ovario maligno de bajo grado; sin embargo, la edad de inicio y la manifestación de los síntomas no pueden distinguirse completamente de ambas estirpes.5
Se estima que durante la década previa al inicio de la enfermedad, la tasa de incidencia global es de 3 por cada 100,000 mujeres al año y se ha observado una tasa de aumento anual del 2.3%.6
Desde el punto de vista estadístico, el 10% de los tumores ováricos se complican por torsión, principalmente tumores benignos, que en orden de frecuencia incluyen: quistes simples, quistes dermoides y cistoadenoma seroso.7 La torsión del quiste ovárico es una de las causas ginecológicas más comunes de abdomen agudo y se considerada una urgencia médica.8 Lo anterior no distingue entre las diferentes edades ni la estirpe histológica, pero se ha reportado que es menos común en las mujeres prepúberes y posmenopáusicas.9
Este artículo expone el caso de una paciente que inició con abdomen agudo secundario a torsión de una tumoración dependiente de un anexo, considerándolo de interés para su estudio luego del reporte histopatológico. Se analiza la bibliografía disponible al respecto, con la finalidad de ampliar el conocimiento de la neoplasia.
CASO CLÍNICO
Paciente de 29 años, nacida de un embarazo gemelar monocorial monoamniótico, con antecedentes ginecoobstétricos de: menarquia a los 13 años, ciclo menstrual regular (30 x 5-6 días), inicio de vida sexual activa a los 21 años, dos parejas sexuales, sin método de planificación familiar al momento del estudio; Papanicolaou hace 5 meses, con reporte negativo para malignidad; sin antecedentes de embarazo previo. Acudió a valoración ginecológica de urgencia por un cuadro de dolor abdominal, de dos semanas de evolución, que al momento de la consulta lo refirió insoportable, impidiendo la deambulación, con subsiguiente afectación del estado general.
A la exploración física se encontraron: tensión arterial 126/76 mmHg, frecuencia cardiaca 116 ppm, frecuencia respiratoria 22 rpm, temperatura 36.7 ºC, SaO del 98% al aire ambiente; peso 62 kg, talla 161 cm. Se percibió con facies de dolor, en posición antiálgica; dificultad para la deambulación, abdomen plano, resistencia de los músculos abdominales, peristalsis abolida, y dolor a la palpación superficial y profunda, principalmente en la fosa iliaca izquierda; sin posibilidad de delimitar tumoraciones abdominales. Al tacto vaginal bimanual: cérvix central, puntiforme, con delimitación de una masa firme en el fondo de saco izquierdo; dolor a la retracción de los anexos izquierdos y datos francos de irritación peritoneal.
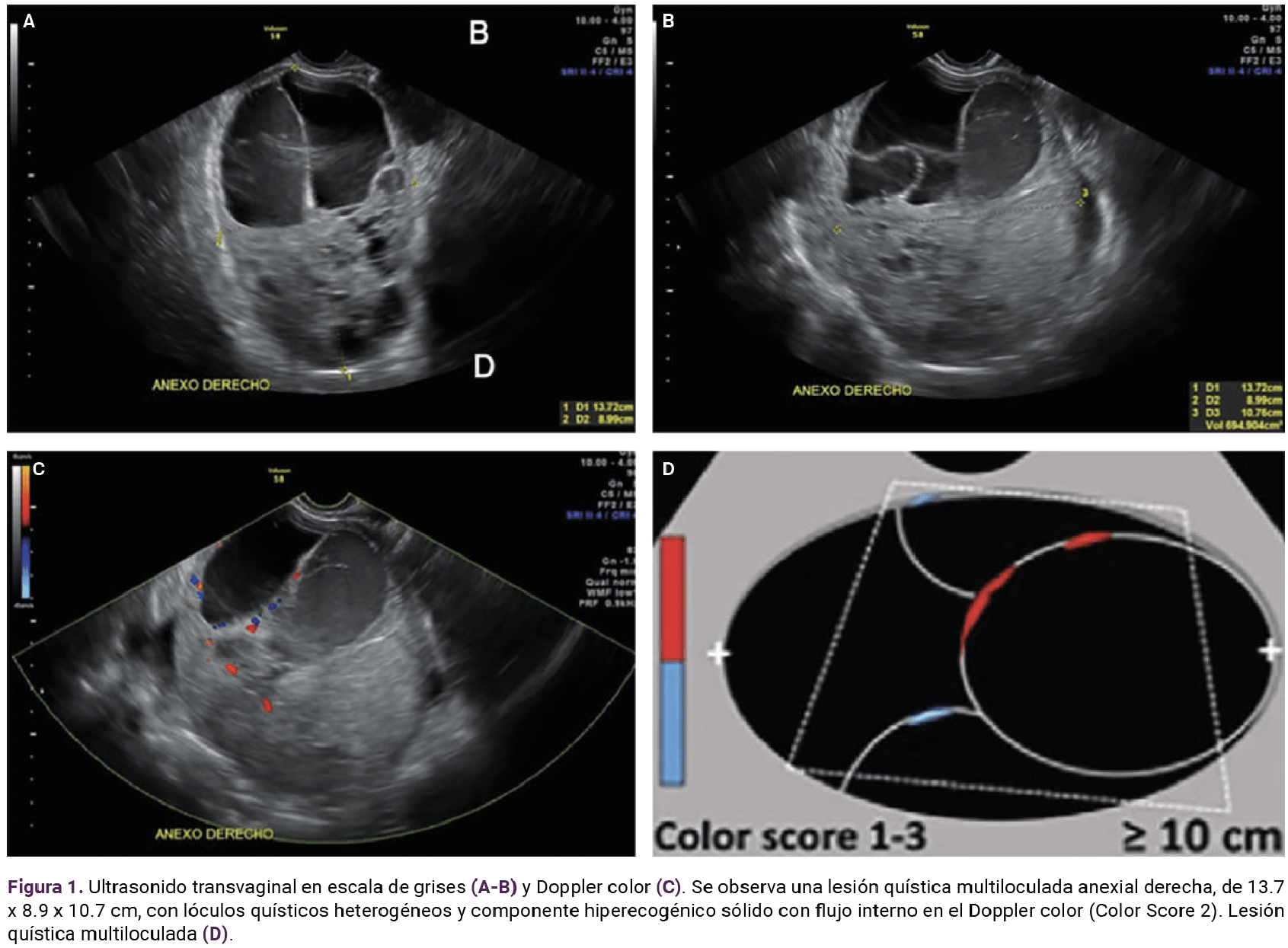
El ultrasonido pélvico reportó datos sugerentes de tumoración compleja, dependiente del ovario izquierdo (Figura 1). Se integró el diagnóstico de abdomen agudo secundario a posible torsión de quiste complejo, dependiente del ovario izquierdo. Se practicó laparotomía exploradora, donde se encontró escaso líquido libre en fondo de saco posterior. Se obtuvieron muestras del líquido y de la tumoración para estudio histopatológico. Posteriormente se procedió a la salpingooforectomía izquierda, con sangrado estimado de 50 mL. Es estudio histopatológico informó: tumor de células de la granulosa de estirpe juvenil. Figuras 2 a 4
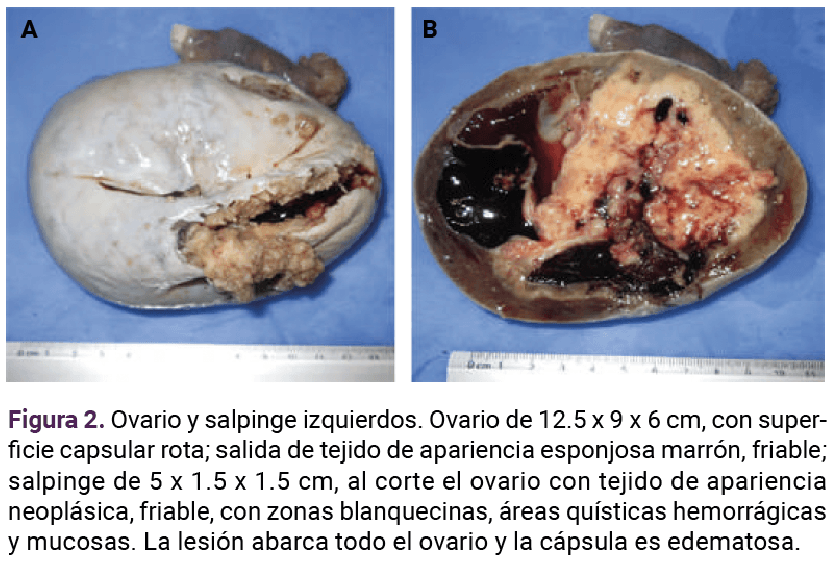
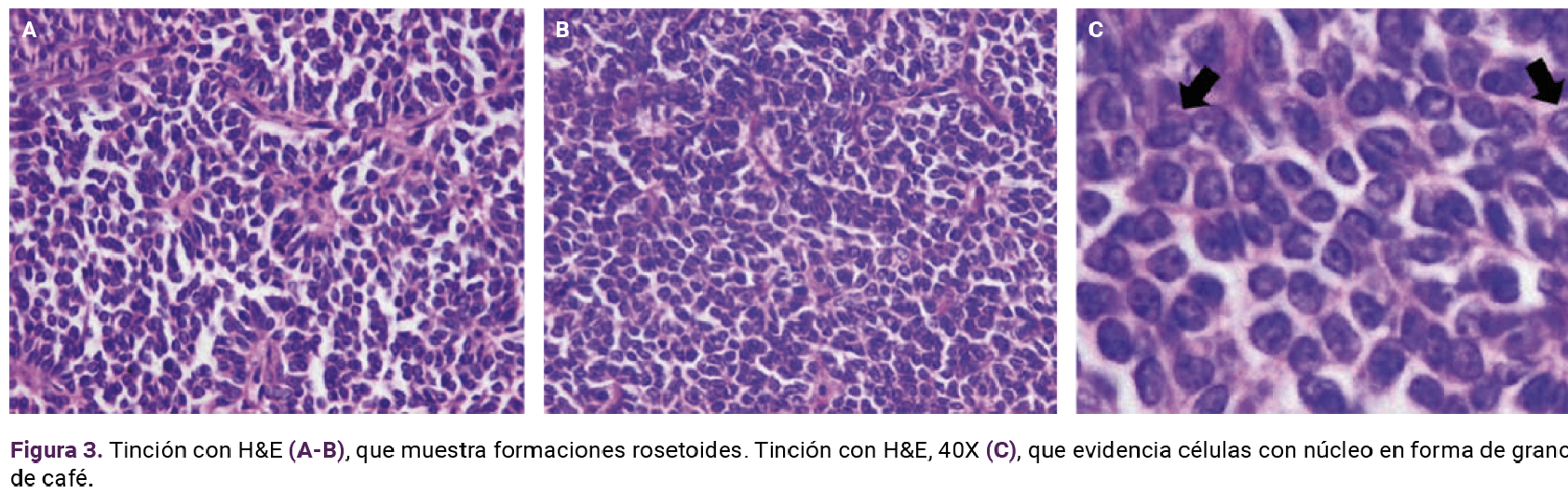
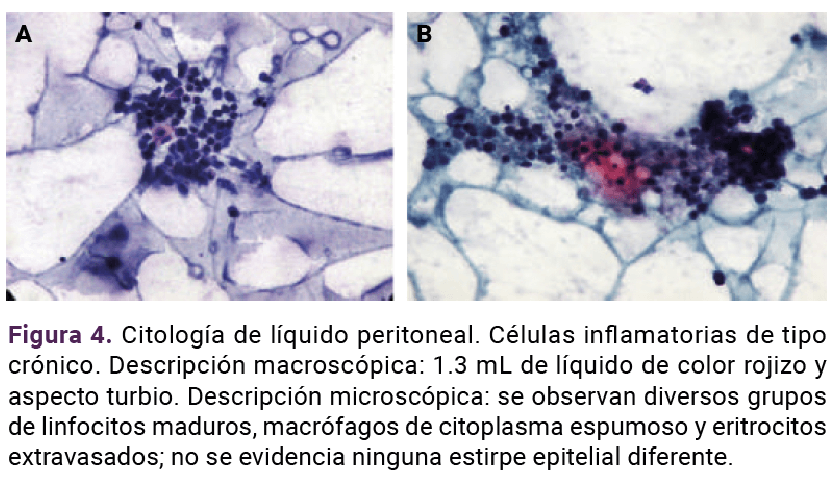
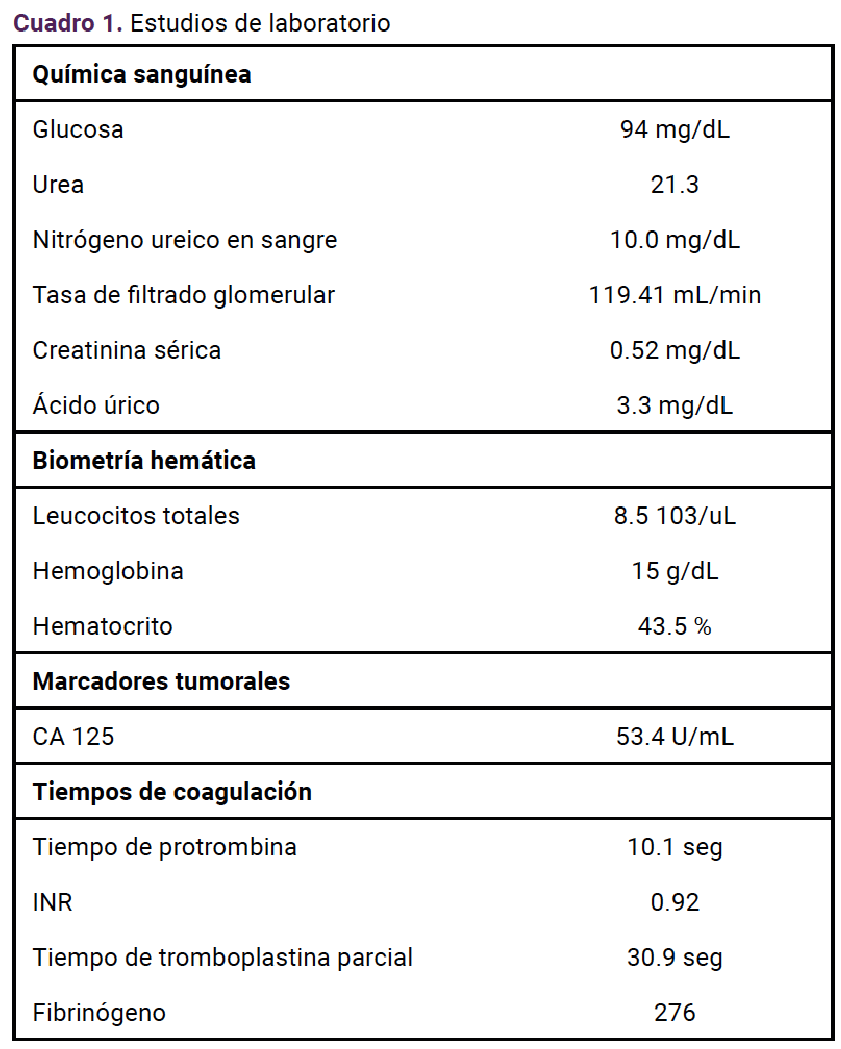
De acuerdo con el diagnóstico establecido por el servicio de Patología, se solicitó una tomografía abdominopélvica, sin hallazgos sugerentes de metástasis, y se obtuvo una biopsia de endometrio, con reporte de endometrio proliferativo, negativo a malignidad. Con la información anterior y de acuerdo con la FIGO 2021 (Cuadro 2), se estadificó en IC2, porque se encontró ruptura de la cápsula del tumor.

Se inició tratamiento adyuvante, con un agente antimicrotubular y taxano; paclitaxel 300 mg y platino; y carboplatino 590 mg, ambos en 6 ciclos. Hoy día la paciente se encuentra en periodo de remisión.
METODOLOGÍA DE BÚSQUEDA
Se llevó a cabo la búsqueda bibliográfica en la base de datos de Medline, vía PubMed, con los términos MeSH: “ovarian tumors”, “ovarian granulosa cell tumors”, “juvenile granulosa cell tumor”, “torsion of ovarian tumors”. La búsqueda se limitó por los siguientes filtros: “Case Reports”, “Review”, “Systematic Reviews”, y “Books and Documents”, “Spanish and English”, desde el año 2003 al 2023.
Se encontraron 2063 estudios, pero se excluyeron editoriales, reseñas, artículos duplicados, para finalmente incluir 38 artículos con diagnóstico histopatológico de tumor de células de la granulosa, tumor de células de la granulosa de estirpe juvenil y torsión de tumoración ovárica.
DISCUSIÓN
Factores de riesgo
Se ha establecido que las mujeres con índice de masa corporal mayor de 30 kg/m2 y quienes tienen antecedente familiar de cáncer de mama o de ovario son más susceptibles de padecer tumor de células de la granulosa. Otro estudio informó que las mujeres con antecedente de consumo crónico de hormonas por vía oral o con antecedente de parto tienen menor riesgo de tumor de células de la granulosa.11
Factores genéticos asociados con el tumor de células de la granulosa
Hace poco se demostró que FOXL212 y las vías de señalización PI3K/AKT,13 TGF-β,14 Notch,15 entre otras, están implicados en la génesis del tumor de células de la granulosa mediante la proliferación celular y apoptosis. Estas vías de señalización no están aisladas, es decir, forman una red compleja y contribuyen a la formación y crecimiento del tumor. FOXL2 es el gen implicado más estudiado y hasta ahora representa el más importante en su formación.16
Manifestaciones clínicas
Los síntomas iniciales más frecuentes son: dolor en el hipogastrio (principalmente irradiado hacia alguna de las fosas iliacas) y sangrado uterino anormal, causado por la secreción exagerada de hormonas que producen las células tumorales.17 También se ha informado distensión abdominal (50%) y ascitis (34%).18 El tumor de células de la granulosa es una neoplasia funcional, por lo que las células tumorales pueden producir estrógenos, lo que conduce a hiperestrogenismo, desarrollo de caracteres sexuales secundarios, aumento del tamaño de las glándulas mamarias, crecimiento de vello púbico y sangrado uterino anormal, dependiendo de la edad de la paciente al momento del diagnóstico.19
Proceso diagnóstico
Si bien el dolor abdominal es la principal manifestación clínica, acompañada de náuseas y vómito, la torsión del tumor ovárico debe considerarse después de obtener una ecografía o tomografía computada que indique una masa dependiente de alguno de los ovarios. De acuerdo con las estadísticas, la correlación entre los hallazgos en los estudios de imagen y la torsión del tumor es del 85%.20 Luego de la sospecha diagnóstica de tumor de ovario con torsión se requiere la exploración quirúrgica inmediata. Hasta ahora no existe un criterio unificado para extirpar o no un ovario con torsión.
Puesto que el tumor de células de la granulosa es excepcional, no existen imágenes uniformes para establecer el diagnóstico. Sin embargo, de acuerdo con los estudios consultados, se encontró ecogenicidad variable entre los diferentes lóculos quísticos, uno demostraba ecos internos de bajo nivel y tabique incompleto, y el resto fueron anecoicos y tenían paredes internas lisas que componían una septación delgada regular. Por su localización e imposibilidad de visualizar el ovario ipsilateral se asumió un origen ovárico, por lo que el componente sólido se describió “heterogéneo e hiperecogénico”, rodeando el parénquima ovárico con pequeños folículos periféricos. Los septos y el componente sólido mostraron un flujo mínimo en el Doppler color (Color score 2). Con base en las características previamente descritas, se clasificó la lesión con categoría de riesgo intermedio de neoplasia maligna O-RADS 4.21,22
El diagnóstico de tumor de células de la granulosa se basa en la histomorfología asistida por immunohistoquímica.23 Las concentraciones séricas elevadas de AMH, inhibina B y hormonas sexuales también contribuyen con el diagnóstico de tumor de células de la granulosa.24 En algunas ocasiones, el tumor de células de la granulosa de estirpe juvenil y otra neoplasias relacionadas tienen características histopatológicas similares a las de la estirpe adulta, lo que hace que el diagnóstico sea difícil de establecer y tenga repercusión importante en la evaluación del tratamiento y el pronóstico.25
Histopatología del tumor de células de la granulosa
Las características patológicas comunes del tumor de células de la granulosa de estirpe adulta son los cuerpos Call-Exner y los surcos nucleares. En cuanto a la estirpe juvenil, se caracteriza por un tumor bien demarcado, con perforación de estructuras papilares, numerosas estructuras similares al folículo, secreciones eosinofílicas delgadas y sin cuerpos Call-Exner o surcos nucleares;26 sin embargo, la estructura folicular no es exclusiva de esta estirpe. Del mismo modo, algunas pacientes con tumor de células de la granulosa de estirpe adulta pueden o no tener cuerpos Call-Exner,4 por lo que es necesario identificar otras manifestaciones patológicas.
Modalidades de tratamiento
La Red Integral del Cáncer (NCCN) y las Guías de la Sociedad Europea de Oncología Médica (ESMO 2018) coinciden en que el tratamiento de referencia en pacientes con tumor de células de la granulosa es la cirugía de estadificación, siempre tomando en cuenta la cirugía de preservación de la fertilidad (sobre todo en pacientes que desean preservar la fertilidad cuando el tumor se limita al ovario).27
Tratamiento quirúrgico
Entre el 60 y 95% de los tumores de células de la granulosa se diagnostican en etapa temprana.17 La cirugía es el tratamiento de primera línea en pacientes recién diagnosticadas y en quienes tienen recurrencia de la enfermedad.
Quimioterapia adyuvante
En la actualidad, la quimioterapia adyuvante con platino se prescribe en pacientes en etapa II-IV, según la FIGO (Federación Internacional de Ginecología y Obstetricia; FIGO 2014), y tumor de células de la granulosa recurrente.17
Tratamiento con preservación de la fertilidad
Comparado con otros tipos de cáncer de ovario epitelial, el tumor de células de la granulosa suele afectar a mujeres jóvenes.31
Recurrencia
El tumor de células de la granulosa suele reportar tasas de recurrencia tardía y múltiple,17 del 20% en etapa IA y del 43 al 48 % en la etapa II-IV.34
Pronóstico y supervivencia
Las pacientes con tumor de células de la granulosa tienen pronóstico favorable y bajo potencial maligno.17
CONCLUSIONES
El tumor de células de la granulosa representa menos del 5% de las neoplasias malignas del ovario: más del 90% de los casos corresponden a la estirpe adulta. En la actualidad, la mayoría de los casos se diagnostica en estadios tempranos de la enfermedad, cuando el tumor suele estar confinado a un solo ovario y la cápsula ovárica permanece intacta. La cirugía estadificadora con estudio anatomopatológico transquirúrgico sigue siendo el protocolo de referencia para el procedimiento inicial. En concordancia con las últimas actualizaciones y estadificación para situaciones clínicas, como la expuesta en este caso, se recomienda un régimen de tratamiento de seis ciclos de carboplatino y paclitaxel. Hoy día el principal desafío radica en el diagnóstico temprano y prevención de la recurrencia, pues esta última aumenta significativamente la supervivencia de las pacientes. La investigación futura debe enfocarse en la identificación y conocimiento de los mecanismos moleculares y desarrollo de tratamientos dirigidos a pacientes con tumor de células de la granulosa.
REFERENCIAS
- Rao AC, Kishore M, Monappa V. Juvenile Granulosa Cell Tumour: Anaplastic Variant with Omental Deposits. J Clin Diagnost Res 2016; 10 (2): ED01-ED3. https://doi.org/10.7860/JCDR/2016/15207.7168
- Schumer ST, Cannistra SA. Granulosa cell tumor of the ovary. J Clin Oncol 2003; 21 (6): 1180-1189. https://doi.org/10.1200/JCO.2003.10.019
- Kalfa N, Fellous M, Boizet-Bonhoure B, Patte C, et al. Aberrant expression of ovary determining gene FOXL2 in the testis and juvenile granulosa cell tumor in children. J Urol 2008; 180 (4): 1810-1813. https://doi.org/10.1016/j.juro.2008.03.124
- Hsu CY, Chang FW, Chao AS, Yu MH, et al. Detection of splice site and frameshift mutations of the FOXL2 gene in juvenile granulosa cell tumors of the ovary. J Gynecol Oncol 2012; 23 (4): 250-254. https://doi.org/10.3802/jgo.2012.23.4.250
- Ouyang P, Li Y, Lin G. A huge juvenile granulosa cell tumor of the ovary presenting as ovary hyperstimulation syndrome and massive ascites in postmenopausal woman. Gynecol Endocrinol 2014; 30 (7): 472-474. https://doi.org/10.3109/09513590.2014.900194
- Mangili G, Sigismondi C, Frigerio L, Candiani M, et al. Unusual -sizes- of ovarian granulosa cell tumors. Gynecol Oncol 2011; 122 (1): 233-234. https://doi.org/10.1016/j.ygyno.2011.03.034
- Zhu Q, Li C, Zhao W, Zhang J, et al. A Rare Case of Ovarian Juvenile Granulosa Cell Tumor. Saudi J Pathol Microbiol 2022; 7 (7): 346-349. https://doi.org/10.36348/sjpm.2022.v07i07.013
- Jones MR, Kamara D, Karlan BY, Phan T, et al. Late Recurrence of Ovarian Granulosa Cell Tumor. J Clin Oncol 2017; 35 (10): 1102-1104. https://doi.org/10.1200/JCO.2016.71.7169
- Evans AT, Gaffey TA, Malkasian GD, Annegers JF. Clinicopathologic review of 118 granulosa and 82 theca cell tumors. Obstet Gynecol 1980; 55 (2): 231-238. PMID: 7352088.
- Dixit S, Singhal S, Baboo HA, Vaidya P, et al. Torsion of ovarian tumor: a clinicopathological review. Indian J Pathol Microbiol. 1989; 32 (2): 96-9. PMID: 2777028.
- Bodurka DC, Deavers MT, Silva EG. Ovarian Sex Cord-Stromal Tumors. In: Hoskins WJ, Perez CA, Young RC. Principles and practice of gynecologic oncology. 4th Ed. Lippincott Williams & Wilkins: Philadelphia. 2005; 1051- 66.
- Jamieson S, Fuller PJ. Management of granulosa cell tumour of the ovary. Curr Opin Oncol 2008; 20 (5): 560-564. https://doi.org/10.1097/CCO.0b013e32830bce56
- Rey RA, Pask AJ, Tüttelmann F, Kliesch S, et al. Repression of Anti-Müllerian hormone expression in the developing human testis by Androgen signaling. J Clin Endocrinol Metab 2016; 101 (9): 3433-3443. https://doi.org/10.1210/jc.2016-1652
- Jamieson S, Alexiadis M, Fuller PJ. Expression status and mutational analysis of Inhibin/Activin subunit genes in granulosa cell tumors of the ovary. Gynecol Oncol 2004; 94 (1): 140-144. https://doi.org/10.1016/j.ygyno.2004.03.049
- McCluggage WG. The pathology of and controversial aspects of ovarian sex cord-stromal tumors. Mod Pathol 2019; 32 (1): 50-60. https://doi.org/10.1038/s41379-018-0150-5
- Pectasides D, Pectasides E, Psyrri A. Granulosa cell tumor of the ovary. Cancer Treat Rev 2008; 34 (1): 1-12. https://doi.org/10.1016/j.ctrv.2007.08.007
- Kottarathil VD, Antony MA, Nair IR, Pavithran K. Recent Advances in Granulosa Cell Tumor Ovary: a review. Indian J Surg Oncol 2013; 4 (1): 37-47. https://doi.org/10.1007/s13193-012-0204-4
- Park JY, Jin KL, Kim DY, Kim JH, et al. Surgical staging and adjuvant chemotherapy in the management of patients with adult granulosa cell tumors of the ovary. Gynecol Oncol 2012; 125 (1): 80-86. https://doi.org/10.1016/j.ygyno.2011.12.020
- Gershenson DM, Morris M, Burke TW, Levenback C, et al. Treatment of poor-prognosis sex cord-stromal tumors of the ovary with the combination of bleomycin, etoposide, and cisplatin. Obstet Gynecol 1996; 87 (4): 527-31. https://doi.org/10.1016/0029-7844(96)00025-9
- Gershenson DM. Management of ovarian germ cell tumors. J Clin Oncol 2007; 25 (20): 2938-2943. https://doi.org/10.1200/JCO.2007.10.8888
- NCCN clinical practice guidelines in oncology. Ovarian Cancer. Including fallopian tube cancer and primary peritoneal cancer. Version 2.2020. https://www.nccn.org/professionals/physician_gls/pdf/ovarian.pdf
- R Pautier, C Lhommé, P Culine, N Duvillard, et al. Adult granulosa-cell tumor of the ovary: a retrospective study of 45 cases. Int J Gynecol Cancer 1997; 7 (1): 58-65. https://doi.org/10.1046/j.1525-1438.1997.00331.x
- Hines JF, Khalifa MA, Moore JL, Fine KP, et al. Recurrent granulosa cell tumor of the ovary 37 years after initial diagnosis: a case report and review of the literature. Gynecol Oncol 1996; 60 (3): 484-488. https://doi.org/10.1006/gyno.1996.0071
- Schumer ST, Cannistra SA. Granulosa cell tumor of the ovary. J Clin Oncol 2003; 21 (6): 1180-1189. https://doi.org/10.1200/JCO.2003.10.019
- Mangili G, Sigismondi C, Frigerio L, Candiani M, et al. Unusual -sizes- of ovarian granulosa cell tumors. Gynecol Oncol 2011; 122 (1): 233-234. https://doi.org/10.1016/j.ygyno.2011.03.034
- Wang D, Cao D, Jia C, Guo L, et al. Analysis of oncologic and reproductive outcomes after fertility-sparing surgery in apparent stage I adult ovarian granulosa cell tumors. Gynecol Oncol 2022; 164 (1): 110-115. https://doi.org/10.1016/j.ygyno.2021.11.012
- van Meurs HS, van Lonkhuijzen LR, Limpens J, et al. Hormone therapy in ovarian granulosa cell tumors: A systematic review. Gynecol Oncol 2014; 134 (1): 196-205. https://doi.org/10.1016/j.ygyno.2014.05.005
- Brown J, Shvartsman H, Deavers MT, Ramondetta LM, et al. The activity of taxanes in the treatment of sex cord-stromal ovarian tumors. J Clin Oncol 2004; 22 (17): 3517-3523. https://doi.org/10.1200/JCO.2004.11.099
- Miller BE, Barron BA, Wan JY, et al. Prognostic factors in adult granulosa cell tumor of the ovary. Cancer 1997; 79 (10): 1951-1955. https://doi.org/10.1002/(SICI)1097-0142(19970515)79:10<1951::AID-CNCR15>3.0.CO;2-D
- Malmström H, Högberg T, Risberg B, Simonsen E. Granulosa cell tumors of the ovary: prognostic factors and outcome. Gynecol Oncol 1994; 52 (1): 50-55. https://doi.org/10.1006/gyno.1994.1009
- Björkholm E, Silfversward C. Prognostic factors in granulosa-cell tumors. Gynecol Oncol 1981; 11 (3): 261-74. https://doi.org/10.1016/0090-8258(81)90061-8
- Suh DS, Kim M, Lee KH, Eom KY, et al. Major clinical research advances in gynecologic cancer in 2016: 10-year special edition. J Gynecol Oncol 2017; 28 (2): e45. https://doi.org/10.3802/jgo.2017.28.e45
- Suri A, Carter EB, Horowitz N, Denslow S, et al. Factors associated with an increased risk of recurrence in women with ovarian granulosa cell tumors. Gynecol Oncol 2013; 131 (2): 321-324. https://doi.org/10.1016/j.ygyno.2013.08.013
- Mangili G, Ottolina J, Gadducci A, Giorda G, et al. Long-term follow-up is crucial after treatment for granulosa cell tumours of the ovary. Br J Cancer 2013; 109 (1): 29-34. https://doi.org/10.1038/bjc.2013.241