RESUMEN
ANTECEDENTES: El embarazo molar parcial, con feto vivo sano coexistente en el segundo trimestre del embarazo es una forma poco frecuente de las molas hidatiformes. La incidencia de complicaciones de los embarazos molares no está suficientemente descrita debido a su baja frecuencia. Se reporta que entre el 1% y el 3.5% de las mujeres con gestaciones molares resultan con preeclampsia. La preeclampsia atípica se identifica con los criterios de gravedad, entre ellos el síndrome de HELLP y la eclampsia. Debido a los pocos casos reportados se carece de guías que marquen la pauta para la atención médica de estas pacientes.
CASO CLÍNICO: Paciente de 30 años, con embarazo molar parcial de 15 semanas asociado con preeclampsia atípica, complicado con eclampsia y síndrome de HELLP con evolución a insuficiencia multiorgánica que ameritó atención multidisciplinaria y tratamiento quirúrgico, con evolución satisfactoria.
CONCLUSIÓN: La coexistencia de mola parcial con feto vivo supone un alto riesgo de desenlaces perinatales adversos: síndrome de HELLP y eclampsia que aumentan la morbilidad y mortalidad maternofetal y pueden condicionar insuficiencia multiorgánica; por tanto, la atención multidisciplinaria es indispensable. La incidencia de estas complicaciones no está suficientemente descrita debido a lo excepcional de los casos; por tanto, es imprescindible reportar estos casos atípicos a fin de documentar la evidencia de la relación entre uno y otro padecimiento.
PALABRAS CLAVE: Embarazo, preeclampsia, eclampsia, HELLP, enfermedad trofoblástica gestacional, embarazo molar parcial
ABSTRACT
BACKGROUND: A partial molar pregnancy with a healthy live fetus in the second trimester is an uncommon form of hydatidiform mole. Due to their low frequency, the incidence of complications with molar pregnancies is not well described. It has been reported that between 1% and 3.5% of women with molar pregnancies develop preeclampsia. Atypical preeclampsia is identified by severity criteria, including HELLP syndrome and eclampsia. Due to the small number of reported cases, there are no established guidelines for the medical care of these patients.
CLINICAL CASE: A 30-year-old patient presented with a 15-week partial molar pregnancy complicated by atypical preeclampsia, eclampsia, and HELLP syndrome. The patient progressed to multiple organ failure and required multidisciplinary care and surgical treatment. The outcome was satisfactory.
CONCLUSION: The coexistence of partial molar pregnancy with a live fetus poses a high risk of adverse perinatal outcomes. HELLP syndrome and eclampsia increase maternal and fetal morbidity and mortality and can lead to multiple organ failure. Therefore, multidisciplinary care is essential. These complications are not well described due to the exceptional nature of the cases. Therefore, reporting these atypical cases is essential to documenting the relationship between the conditions.
KEYWORDS: Pregnancy, Preeclampsia, Eclampsia, HELLP, Gestational trophoblastic disease, Partial molar pregnancy
ANTECEDENTES
La mola hidatidiforme, o embarazo molar, es la consecuencia de una alteración genética que se produce en el momento de la fecundación.1 Es parte de las enfermedades trofoblásticas gestacionales y es su forma más benigna.1 Se origina cuando el tejido que normalmente forma el embrión y la placenta crece anormalmente en el interior del útero y da lugar a unos quistes.1 Este crecimiento anormal de tejido no es advertido por la paciente, pues solo experimenta los síntomas de un embarazo normal.1 La mola hidatiforme se clasifica en completa (sin tejido fetal con proliferación anormal de las vellosidades coriales) o parcial (con posible tejido fetal y casi siempre malformaciones debidas a las anomalías cromosómicas).2 La incidencia de mola parcial es de 3 casos por cada 1000 embarazos3 y la de la coexistencia de feto vivo con mola parcial es de 1 caso por cada 22,000 a 100,000 gestaciones.4
La mayor parte de las molas completas son diploides de origen paterno, homocigotas 46 XX en el 90% de los casos y heterocigotas 46 XY en el otro 10%.5 Las molas parciales suelen ser triploides biparentales, con cariotipo 69 XXY (70%), 69 XXX (27%) o 69 XYY (3%).5 La frecuencia de embarazos molares en México es de 2.4 por cada 1,000 gestaciones.6 Menos de la mitad de los casos (43%) se diagnostican como hallazgo en la ecografía de rutina practicada en las primeras semanas de embarazo.6
Los síntomas de los embarazos molares pueden incluir: sangrado vaginal, náuseas y vómitos intensos, crecimiento uterino rápido, dolor y presión pélvica e hipertensión arterial.7 También pueden presentarse hiperémesis, preeclampsia y eclampsia, hipertiroidismo, muerte fetal intrauterina inexplicable o restricción del crecimiento fetal, parto prematuro o rotura prematura de membranas y dolor pélvico.7
Los factores de riesgo son: la edad, la etnia, los antecedentes de embarazos molares y familiares.8 También contribuyen al perfil de riesgo los antecedentes médicos caracterizados por abortos espontáneos o infertilidad, consideraciones dietéticas, el tabaquismo, el grupo sanguíneo B, la edad del padre, las anomalías genéticas de la madre y la anticoncepción hormonal oral.8 Las complicaciones médicas ocurren en alrededor del 25% de las pacientes con agrandamiento uterino mayor a un tamaño gestacional de 14 a 16 semanas, pero con menor frecuencia en pacientes con útero más pequeño.8
El embarazo gemelar con mola y feto vivo se asocia con un aumento de complicaciones maternas: preeclampsia en 20 a 30%, sangrado vaginal en 46% e hiperémesis gravídica en 17%.9 Si bien la preeclampsia y el síndrome HELLP pocas veces se inician antes de las 20 semanas de embarazo, los informes sugieren apariciones tempranas de estos trastornos hipertensivos, de manera particular en el contexto de un embarazo molar.10 En el 27% de los casos de molas hidatiformes no tratadas la preeclampsia aparece en el segundo trimestre.11
La eclampsia es una de las complicaciones agudas más graves del embarazo que implica una alta morbilidad y mortalidad para la madre y el recién nacido.12 Las pacientes con eclampsia tienen mayor riesgo de complicaciones graves: desprendimiento de placenta, síndrome HELLP, coagulación intravascular diseminada, edema pulmonar, neumonía por aspiración, paro cardiopulmonar e insuficiencia renal aguda.12 La incidencia de eclampsia en pacientes con embarazos molares no se ha descrito debido a su baja frecuencia.13 Se reporta que entre el 1% y el 3.5% de las embarazadas con gestaciones molares padecen preeclampsia.13
CASO CLÍNICO
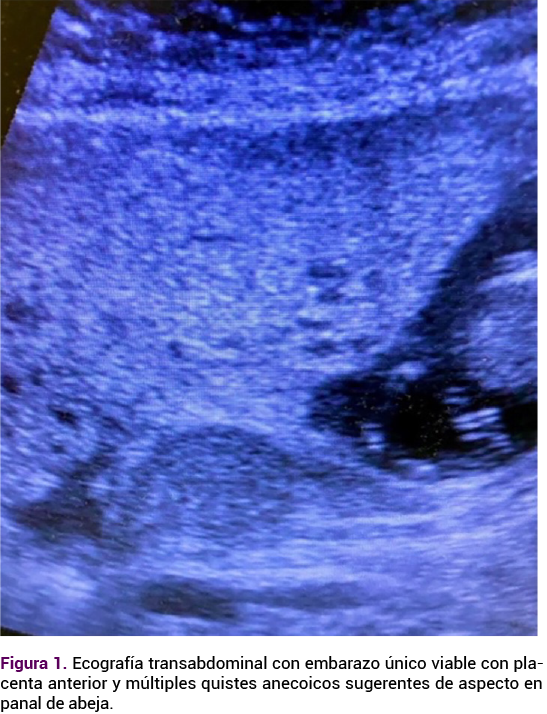
Paciente de 30 años, con antecedente de dos embarazos y una cesárea en curso de las 15 semanas de gestación, que acudió a urgencias debido a un dolor abdominal epigástrico, con náuseas y vómitos de tres días de evolución; sin control prenatal, obesidad mórbida, peso de 110 kg y altura de 1.57 m, con fondo uterino por encima de la sínfisis del pubis. La ecografía transabdominal confirmó un embarazo único viable, compatible con 14.5 semanas de gestación mediante biometría fetal, con latido fetal audible y una placenta anterior agrandada, con múltiples quistes anecoicos, de aspecto en panal de abeja y oligohidramnios. Además, múltiples quistes tecaluteínicos sugerentes de enfermedad trofoblástica compatible con mola hidatiforme parcial.
La paciente se encontró con tensión arterial superior a 160-110 mmHg en repetidas mediciones, compatibles con preeclampsia grave. Se decidió su hospitalización para la estabilización, práctica de más estudios y cuantificación de la βhGC. Una hora posterior al tratamiento antihipertensivo, la paciente tuvo una convulsión tónico-clónica generalizada de 60 segundos de duración, sin signos neurológicos focales. La convulsión se trató con una dosis de carga de 6 g de sulfato de magnesio y una dosis de mantenimiento de 2 g por hora, junto con hidralazina y bloqueadores de los canales de calcio.
Se estableció el diagnóstico de eclampsia asociada con enfermedad trofoblástica gestacional. Se le indicaron sulfato de magnesio con esquema de Zuspan para prevenir y tratar las convulsiones; además, 400 μg cada 4 horas de misoprostol por vía vaginal para incentivar la maduración cervical.
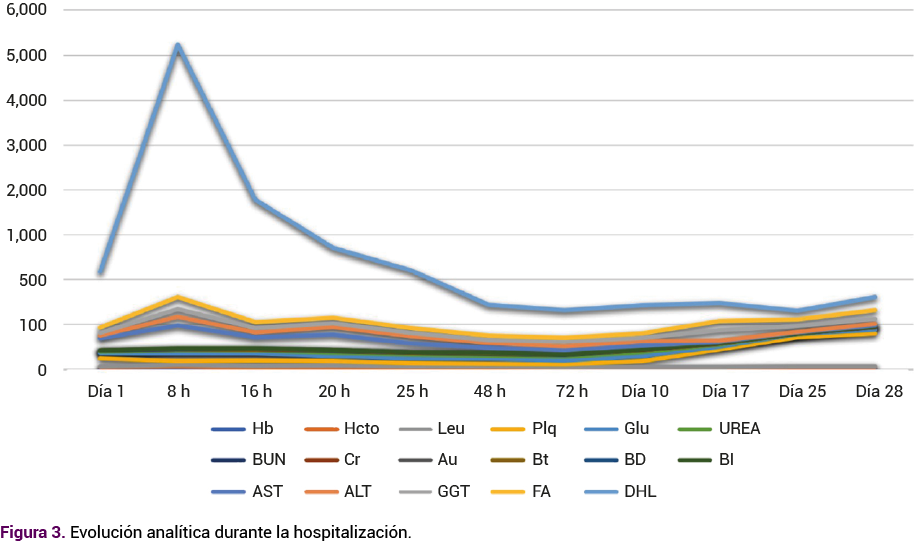
Los análisis de laboratorio reportaron: hematocrito: 49.2% ALT: 262 U/L; AST: 625 U/L; LDH: 1251 U/L; plaquetas: 90,000/μL; creatinina: 1.7 mg/dL; bilirrubina total: 0.9 mg/dL; bilirrubina directa: 0.5 mg/dL; bilirrubina indirecta: 0.4 mg/dL; proteínas en análisis de orina: 500 mg/dL; β-hCG: 624.660 mUI/mL. Con estos reportes se confirmó la enfermedad trofoblástica gestacional y el síndrome HELLP que evolucionó a las 16 horas de su internamiento con los siguientes valores de control bioquímico: ALT: 512 U/L; AST: 2033 U/L; LDH: 5637 U/L; plaquetas: 90,000/μL; creatinina: 1.7 mg/dL; bilirrubina total: 6.4 mg/dL; bilirrubina indirecta: 4.1 mg/dL; bilirrubina directa: 2.3 mg/dL; hipertransaminasemia e hiperbilirrubinemia a expensas de la bilirrubina indirecta que evolucionó a insuficiencia hepática aguda, clasificación III.
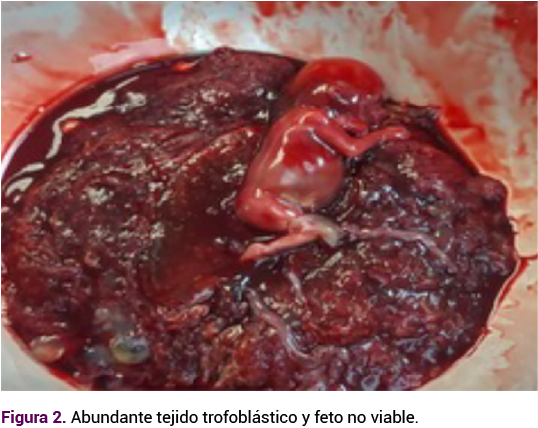
Doce horas posteriores a la maduración, debido al estado de gravedad y modificaciones cervicales no favorables, se procedió a la laparotomía exploradora en la que se encontró abundante ascitis de alrededor de 500 cc, petequias en el peritoneo parietal y en el hígado, además del útero aumentado de tamaño para las semanas de gestación. Debido a la paridad no satisfecha se optó por la histerotomía evacuadora, con obtención de abundante tejido trofoblástico y un feto intrauterino no vivo.
Durante el periodo transquirúrgico la paciente cursó con signos vitales con tendencia a la hipotensión; se indicaron aminas y soporte respiratorio (ventilación mecánica invasiva) y atención multidisciplinaria. Enseguida se trasladó a la unidad de cuidados intensivos con prescripción de valproato de magnesio y fluidoterapia guiada por objetivos. La TAC de cráneo, tórax y abdomen se reportó negativa para signos de efecto de masa, hemorragia o isquemia, sin evidencia de metástasis.
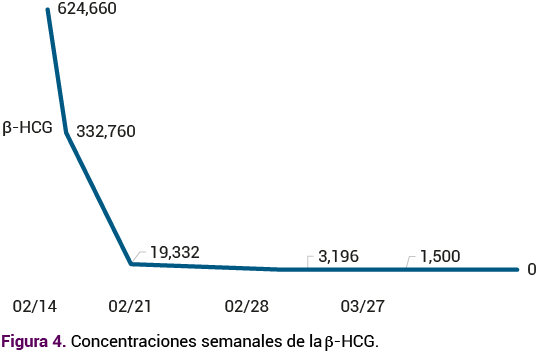
Cinco días más tarde, el estudio histopatológico del tejido placentario demostró degeneración hidrópica parcial, feto femenino de 8.6 cm de longitud cefalocaudal, con hemorragia en la extremidad pélvica izquierda. Durante la hospitalización continuó con evolución hacia la insuficiencia renal, a pesar del tratamiento con diuréticos. Ameritó soporte renal en cuatro ocasiones y se decidió la traqueostomía al decimoquinto día en la unidad de cuidados intensivos para uso prolongado de ventilación mecánica invasiva, con mantenimiento de las cifras tensionales en metas terapéuticas, en tratamiento con telmisartán-hidroclorotiazida y nifedipino, con mejoría significativa del hemograma, función renal y con tendencia al descenso de las concentraciones de enzimas hepáticas con remisión del síndrome de HELLP y de la insuficiencia renal, descenso de las concentraciones de cuantificación semanal de la β−hGC hasta su negativización. La paciente se dio de alta de la unidad de cuidados intensivos a los 20 días posteriores a la intervención quirúrgica y 4 días más tarde del hospital, con seguimiento en la consulta externa.
DISCUSIÓN
Las pautas actuales de tratamiento para el embarazo molar se centran principalmente en la evacuación del embarazo y la vigilancia estricta de la β-HCG para prevenir el avance a neoplasia gestacional.10-14 Por lo que se refiere a la atención médica del embarazo molar con feto vivo, algunos autores recomiendan la amniocentesis para determinar el cariotipo fetal.14 En las primeras etapas del embarazo, Bruchim recomienda su finalización cuando el diagnóstico se establece durante la primera mitad de la gestación.14 Si de antemano se sospecha debe evacuarse lo antes posible enseguida de una breve evaluación y estabilización de cualquier complicación.14 En pacientes seleccionadas que no desean preservar la fertilidad, la histerectomía es una opción a la dilatación y evacuación por succión para el retiro de la mola, sobre todo en pacientes mayores de 40 años que, por edad, tienen mayor riesgo de neoplasia trofoblástica gestacional posmolar.15
La fisiopatología de los trastornos del espectro de la eclampsia en el embarazo molar es compleja y multifactorial.16 Algunos estudios recientes evidencian el papel del desequilibrio del factor angiogénico, que cobra interés cuando se combina con la observación de que las placentas molares producen altas concentraciones de factores antiangiogénicos.16 Varios estudios indican que un desequilibrio entre factores angiogénicos, como el factor de crecimiento endotelial vascular (VEGF) y factores antiangiogénicos, como la endoglina soluble y el sFlt-1, puede participar en la patogénesis de las complicaciones del embarazo, incluida la mola hidatiforme y la preeclampsia.16 Se ha encontrado una mayor expresión de sFlt-1 en la sangre y la placenta en pacientes con mola hidatiforme.16
Está demostrado que los restos trofoblásticos de los embarazos molares también inducen la activación de las células endoteliales a través de la proteína de choque térmico 70 (HSP70), expresada en una placenta molar hidatiforme, que puede ser una señal patógena para las células endoteliales.17
El caso aquí reportado demuestra que las pacientes con embarazos molares también corren el riesgo de manifestaciones graves de preeclampsia atípica.17 La paciente del caso resultó con eclampsia y síndrome HELLP antes de las 20 semanas de gestación.17 La estabilización de la paciente se decidió con antihipertensivo, neuroprotección, esquema de maduración cervical para dilatación y evacuación como lo marcan las pautas actuales.10-14 Sin embargo, el deterioro fue evidente, con evolución rápida hacia la insuficiencia multiorgánica debido al síndrome de HELLP.17 Por tanto, se procedió a la laparotomía exploradora e histerotomía, con gestión multidisciplinaria que fue satisfactoria.17
CONCLUSIONES
La coexistencia de una mola parcial, con feto vivo, supone un alto riesgo de desenlaces perinatales adversos, entre ellos el síndrome de HELLP y la eclampsia, que aumentan la morbilidad y mortalidad materna y fetal. En la bibliografía no se encuentra descrita la incidencia de estas complicaciones debido a los pocos casos; sin embargo, la aparición de un cuadro súbito y agudo en el segundo trimestre del embarazo puede suponer una evolución rápida hacia la insuficiencia multiorgánica. La atención de estos casos requiere de un equipo multidisciplinario para su resolución inmediata y tratamiento, por ello es decisivo reconocer los casos atípicos a fin de asentar evidencia de tal asociación de estas afecciones.
REFERENCIAS
- Buyukkurt S, Fisher RA, Vardar MA, Evruke C. Heterogenity in recurrent complete hydatidiform mole: of two new Turkish families with different genetic characteristics. Placenta 2010; 31: 1023-5. https://sci-hub.se/ https://doi.org/10.1016/j.placenta. 2010.09.003
- Joneborg U. Epidemiology of gestational trophoblastic disease. Hematol Oncol Clin North Am 2024; 38 (6): 1173-1190. https://www.sciencedirect.com/sdfe/pdf/download/eid/1-s2.0-S0889858824000807/first-page-pdf
- Seckl MJ, Sebire NJ, Berkowitz RS. Gestational trophoblastic disease. Lancet 2010; 376 (9742): 717-29. https://doi.org/10.1016/S0140-6736(10)60280-2
- Vejerslev LO. Clinical management and diagnostic possibilities in hydatidiform mole with coexistent fetus. Obstet Gynecol Surv 1991; 46 (9): 577-88. https://sci-hub.se/https://doi.org/10.1097/00006254-199109000-00001
- Porras-Ibarra GD, Santiago-Sanabria L, Martinez-Villafaña E, Porras-Zaragoza JL, et al. Mola hidatidiforme parcial con feto vivo sano a término. Ginecol Obstet Mex 2023; 91 (6): 462-467. https://doi.org/10.24245/gom.v91i6.8069
- Lira-Plascencia J, Tenorio-González F, Gomezpedroso-Rea J, et al. Enfermedad trofoblástica gestacional. A seis años de experiencia en el Instituto Nacional de Perinatología. Ginecol Obstet Mex 1995; 63: 478-82.
- Mangla M, Kaur H, Khoiwal K. Partial mole with coexistent live fetus: A systematic review of case reports. J Turk Ger Gynecol Assoc 2022; 23 (2): 83-94. https://doi.org/10.4274/jtgga.galenos.2022.2021-9-11
- Soper JT. Gestational trophoblastic disease: current evaluation and management. Obstet Gynecol 2021; 137 (2): 355-70. https://doi.org/10.1097/AOG.0000000000004240. Erratum in: Obstet Gynecol 2022; 139 (1): 149. https://doi.org/10.1097/AOG.0000000000004589
- Camacho-Montaño AM, Niño-Alba R. Mola parcial con feto vivo, complicado con restricción de crecimiento intrauterino y preeclamsia severa. Reporte de caso y revisión de la literatura. Rev colomb obstet ginecol 2020; 71 (3): 286-89. https://revista.fecolsog.org/index.php/rcog/article/view/3461
- Core D, Vervaeke H, Leethy K, et al. Eclampsia, HELLP y PRES in a 16-week partial molar pregnancy. BMJ Case Rep 2023. https://doi.org/10.1136/bcr-2023-258188
- Salazar Marcatoma L, Osorio Gutiérrez G, Sarmiento Sulca S. Mola hidatiforme completa y preeclampsia severa a las 09 semanas de gestación: reporte de un caso. Ciencia Latina Revista Científica Multidisciplinar 2022; 6 (4): 4939949. https://doi.org/10.37811/cl_rcm.v6i4.2985
- Fishel Bartal M, Sibai BM. Eclampsia in the 21st century. Am J Obstet Gynecol 2022; 226 (2S): S1237-S1253. https://doi.org/10.1016/j.ajog.2020.09.037
- Selamé G, Rodrigo et al. Eclampsia como manifestación clínica de enfermedad trofoblástica gestacional: Reporte de caso. Rev ANACEM 2017. http://ojs.revistaanacem.cl/index.php/anacem/article/view/128
- Bruchim I, Kidron D, Amiel A, Altaras M, et al. Mola hidatiforme completa y feto viable coexistente: reporte de dos casos y revisión de la literatura. Gynecol Oncol 2000; 77 (1): 197-202. https://doi.org/10.1006/gyno.2000.5733
- Soper JT. Gestational trophoblastic disease: current evaluation and management. Obstet Gynecol 2021; 137 (2): 355-70. https://doi.org/10.1097/AOG.0000000000004240
- Marín R, Chiarello DI, Abad C, Rojas D, et al. Estrés oxidativo y disfunción mitocondrial en la preeclampsia de inicio temprano y tardío. Biochim Biophys Acta Mol Basis Dis 2020; 1866 (12): 165961. https://doi.org/10.1016/j.bbadis.2020.165961
- Zhao M, Yin Y, Wei J, Wu M, et al. Trophoblastic debris extruded from hydatidiform molar placentae activates endothelial cells: Possible relevance to the pathogenesis of preeclampsia. Placenta 2016; 45: 42-9. https://doi.org/10.1016/j.placenta.2016.07.007