RESUMEN
ANTECEDENTES: La pandemia de COVID-19 ha tenido una gran repercusión mundial no solo por lo inesperado de sus consecuencias sino por las múltiples enfermedades que sigue generando en el largo plazo. La incidencia de enfermedades autoinmunes, entre ellas las que afectan al sistema nervioso central, se ha incrementado. La encefalitis autoinmune, mediada por receptores anti-N-metil-D-aspartato (NMDAR) es la forma más común de encefalitis, con una estrecha asociación con la coexistencia de tumores, sobre todo teratomas.
CASO CLÍNICO: Paciente de 30 años, nuligesta, con diagnóstico de encefalitis autoinmune mediada por receptores anti-N-metil-D-aspartato (NMDAR), con teratomas bilaterales y antecedente de contagio con SARS-CoV-2 y posterior aplicación de la vacuna Sputnik en México. Debido a que aún se encontraba en edad reproductiva se decidió el tratamiento quirúrgico conservador, con resección de los teratomas y disminución parcial de los síntomas y regreso de éstos que produjeron un deterioro progresivo. En un segundo tiempo quirúrgico se procedió a la ooforectomía bilateral, con la que sí se consiguió una disminución importante de los síntomas.
CONCLUSIÓN: Si bien la incidencia de la encefalitis autoinmune es poco frecuente, no por ello deja de ser relevante; es importante saber que existe una relación directa entre la afección neurológica y la ovárica y que el tratamiento quirúrgico es la piedra angular para conseguir la mejoría clínica de estas pacientes.
PALABRAS CLAVE: Encefalitis autoinmune, teratomas bilaterales, encefalitis autoinmune antirreceptores Anti-N-metil-D-aspartato, teratoma, reporte de caso
ABSTRACT
BACKGROUND: The COVID-19 pandemic has had a major global impact, not only because of the unexpectedness of its consequences, but also because of the multiple diseases it continues to generate in the long term. The incidence of autoimmune diseases, including those affecting the central nervous system, has increased. Anti-N-methyl-D-aspartate receptor (NMDAR) autoimmune encephalitis is the most common form of encephalitis and is closely associated with the coexistence of tumors, especially teratomas.
CLINICAL CASE: 30-year-old patient, nulligravida, diagnosed with anti-N-methyl-D-aspartate receptor (NMDAR) autoimmune encephalitis, with bilateral teratomas and a history of SARS-CoV-2 infection and subsequent use of Sputnik vaccine in Mexico. As she was still of reproductive age, conservative surgical treatment was chosen, with resection of the teratomas and partial reduction of symptoms, which then returned with progressive deterioration. In a second surgical procedure, bilateral oophorectomy was performed, which resulted in a significant reduction of symptoms.
CONCLUSION: Although the incidence of autoimmune encephalitis is rare, it is still relevant. It is important to know that there is a direct relationship between neurological and ovarian disease and that surgical treatment is the cornerstone for achieving clinical improvement in these patients.
KEYWORDS: Autoimmune encephalitis, Bilateral teratomas, Anti-N-methyl-D-aspartate, Receptor encephalitis, Teratoma
ANTECEDENTES
CASO CLÍNICO
Paciente, enviada al servicio de biología de la reproducción por tumoraciones bilaterales dependientes del ovario.
Paciente de 30 años, nuligesta, con inicio del padecimiento en 2022, posterior a la aplicación de la vacuna Sputnik contra COVID-19. Inició con movimientos involuntarios iniciados en las extremidades superiores y propagados a todo el cuerpo, acompañados de alteración en el lenguaje (bradilalia), sin pérdida del estado de alerta, con periodo postictal que condicionaba la limitación en la movilidad, con dependencia de un cuidador. Fue referida al Hospital del Centro Médico Nacional Siglo XXI en donde hicieron una evaluación médica exhaustiva en virtud del amplio diagnóstico diferencial; incluyó: causas infecciosas, inflamatorias, autoinmunes y endocrinas. Se practicaron estudios de gabinete para evaluación del sistema nervioso central. El electroencefalograma no mostró alteraciones. El análisis del líquido cefalorraquídeo se reportó normal. En la resonancia magnética de cráneo se identificó una lesión hiperintensa en la parte frontal derecha y adyacente a la pared del ventrículo lateral izquierdo.
Luego de las pruebas complementarias de diagnóstico, en el líquido cefalorraquídeo se identificaron anticuerpos positivos anti-NMDA y anti-GAD; se le indicó tratamiento con IgG intravenosa a la dosis de 0.4 g/kg.
El tratamiento también incluyó: 75 mg de pregabalina, 0.5 mg de lorazepam, 400 mg de valproato de magnesio, los tres cada 24 horas. Las dosis se modificaron conforme a la evolución clínica de la paciente. El procedimiento diagnóstico también incluyó un ultrasonido pélvico, en el que se encontraron tumoraciones bilaterales, dependientes del ovario. Por ello se envió a la unidad de Ginecología y Obstetricia. Puesto que la paciente manifestó su deseo de preservar la fertilidad fue atendida en el servicio de Biología de la Reproducción.
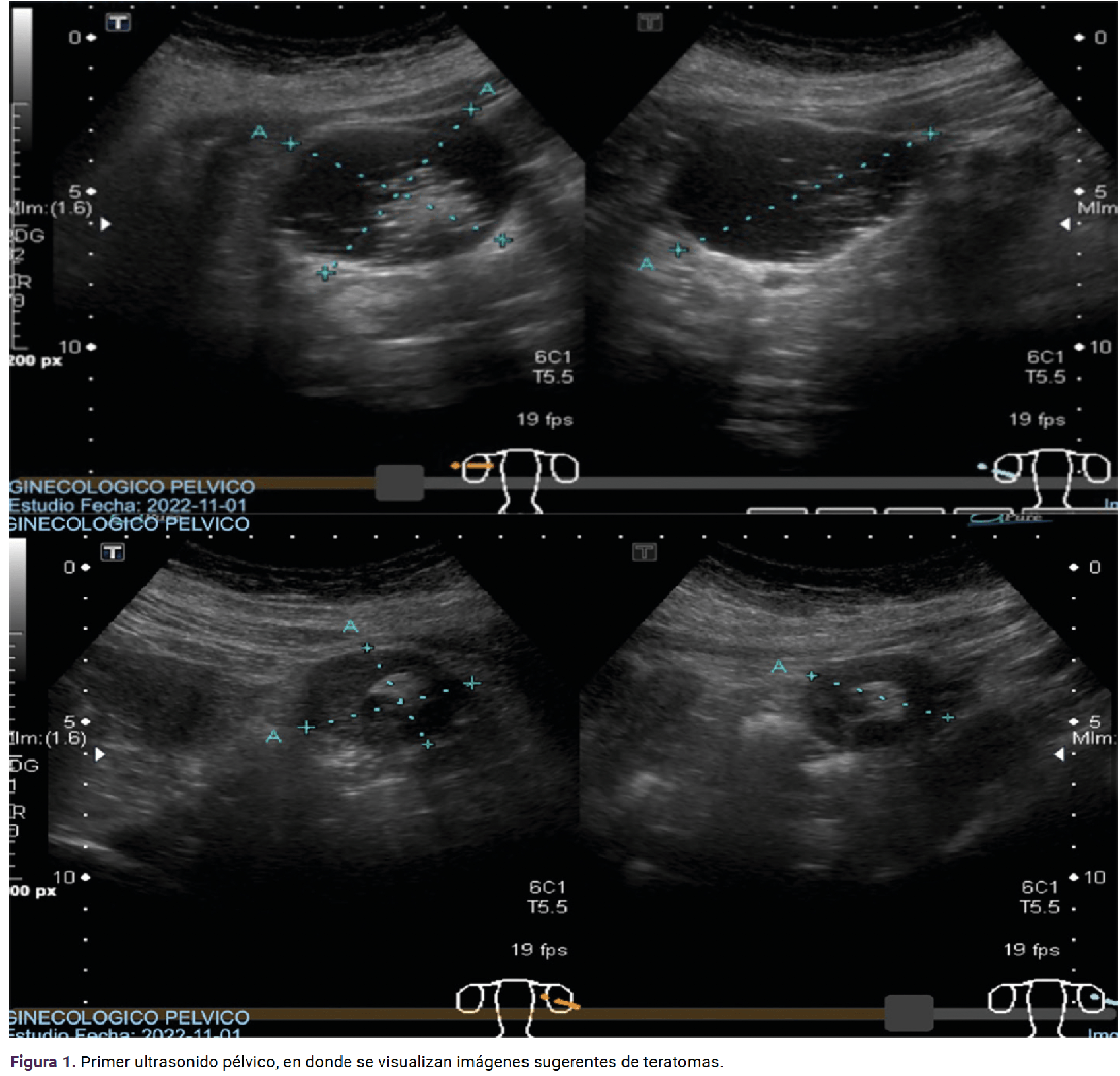
Los estudios de laboratorio reportaron: hemoglobina 13.8 g/dL; hematocrito 44.7%; plaquetas 191/mm3; glucosa 187 mg/dL; urea 14.9 mg/dL; creatinina 0.6 mg/dL, ácido úrico 6.6 mg/dL, CA 125 8.7 U/mL, ACE 1.1 ng/mL, AFP 1.06 ng/mL. El estudio de imagen describió: (Figura 1) útero en anteversoflexión, lateralizado a la derecha 81 x 34 x 51 mm, endometrio 7 mm, ovario derecho 63 x 60 x 71 mm, volumen de 141 cc, estroma completamente alterado con líquido predominante y dos nódulos murales altamente ecogénicos en su interior; el primero de 21 x 19 x 21 mm, el segundo izquierdo y medial de 12 x 12 x 12 mm sin flujo Doppler. El ovario izquierdo 42 x 34 x 25 mm, volumen 27 cc. En su interior se encontró líquido hipoecoico rodeado de un nódulo mural de 16 x 12 x 17 mm sin flujo Doppler. Las imágenes eran sugerentes de teratomas.
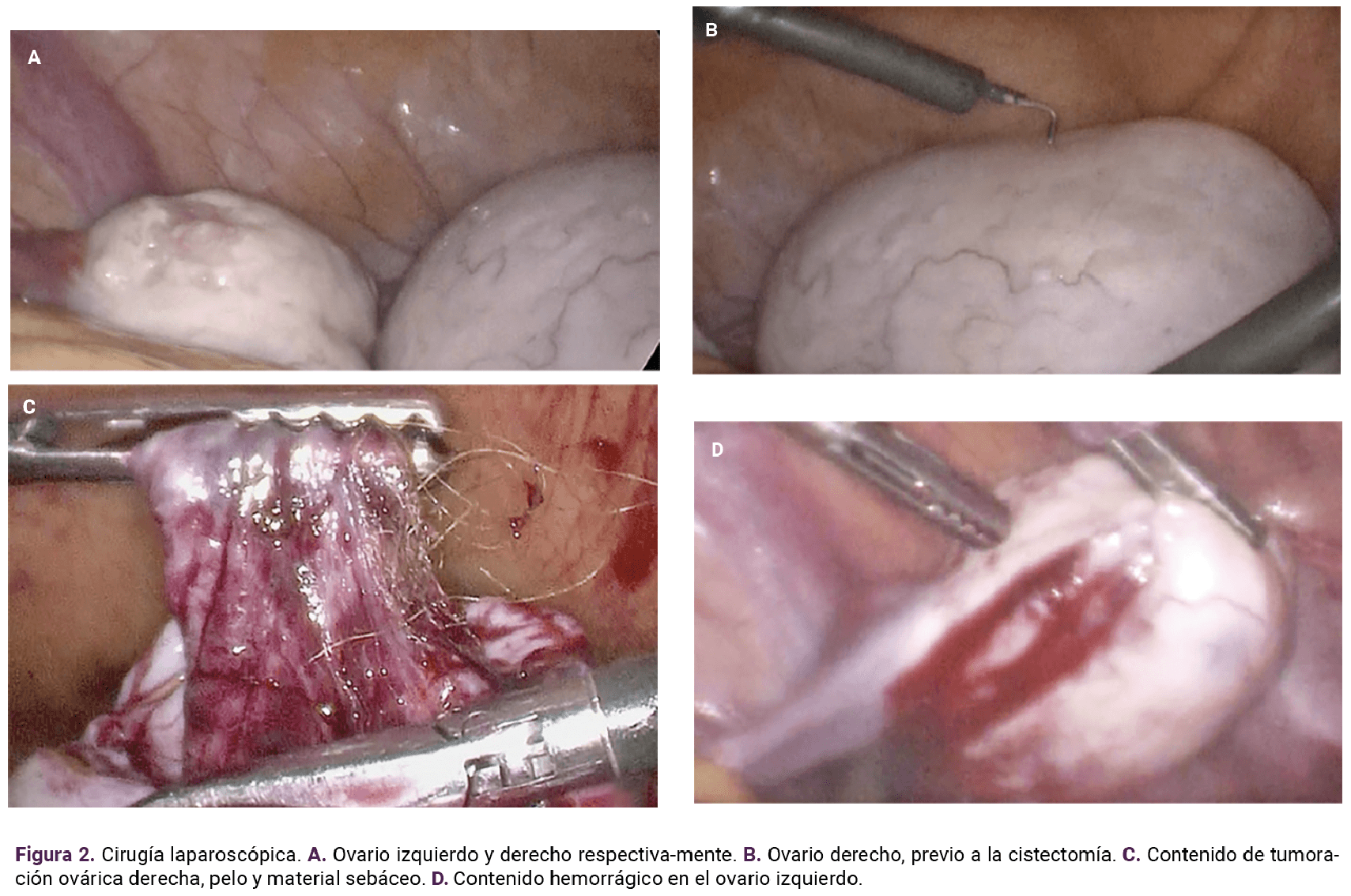
El reporte histopatológico (Figura 2) de la cistectomía bilateral fue: teratoma quístico maduro, con escasa congestión vascular, tumoración izquierda, cuerpo amarillo hemorrágico, con inflamación crónica específica y escasa congestión vascular.
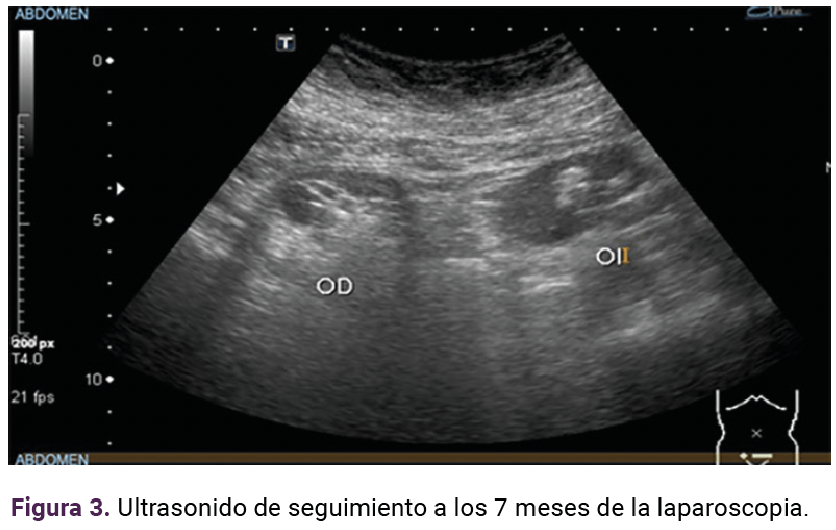
Durante el perido posquirúrgico la paciente permaneció en seguimiento en el servicio de Biología de la reproducción, con disminución de los episodios convulsivos. A los siete meses experimentó una exacerbación del cuadro convulsivo, con aumento en la frecuencia, episodios cada 48 a 72 horas que afectaban por completo la calidad de vida. En otro ultrasonido (Figura 3) se encontró la evidencia de un quiste de 42 mm en el ovario derecho y una imagen mixta, de predominio ecogénico, de 30 x 21 x 32 mm, volumen de 11 cc y 77 x 50 x 63 mm. El ovario izquierdo con una imagen quística de 18 x 12 x 8 mm, volumen 2.6 cc, imagen redondeada ecogénica de 15 x 9 x 13 mm.
Debido a la estrecha relación entre encefalitis autoinmunitaria y teratomas, y el riesgo de recidiva, se decidió la salpingooforectomía bilateral.
En la segunda cirugía (laparotomía) el útero se encontró de 8 y 6 cm, con bordes regulares. Ambas salpinges de características macroscópicas normales, de aproximadamente 10 cm, el ovario derecho de 5 x 4 cm, blanco nacarado, de consistencia firme, en porción periférica con un nódulo sólido, delimitado, de 2 cm. El ovario izquierdo de 4 x 4 cm de consistencia blanda, blanco nacarado, con quiste hemorrágico y contenido aparente líquido. El examen de patología reportó: cistadenofibroma derecho mucinoso y teratoma izquierdo quístico maduro.
En la actualidad, la paciente permanece en seguimiento multidisciplinario, en los servicios de Biología de la reproducción y Neurología, con remisión de los síntomas neurológicos. Aún refiere eventos de crisis convulsivas: un episodio cada mes, tónico clónico localizado, sin alteración del lenguaje, con reincorporación a sus actividades, completamente independiente. Continúa en tratamiento farmacológico con: 600 mg de ácido valproico, 1000 mg de levetiracetam, 500 mg de vigabatrina, pregabalina 75 mg, 1 g de azatioprina, 50 mg de sertralina todos en pauta cada 12 h. Continúa en seguimiento debido al síndrome climatérico inducido quirúrgicamente.
DISCUSIÓN
Se trata de un caso relacionado con encefalitis autoinmune y teratomas bilaterales. No quedó claro si el detonante fue el contagio de COVID-19 o la administración de la vacuna. Lo que sí es evidente es que la piedra angular del tratamiento de estos casos es quirúrgico.
La encefalitis anti-NMDAR se manifiesta, típicamente, como un deterioro clínico de múltiples fases, resultante de una disminución progresiva de la función NMDAR debida a la pérdida de los receptores de superficie de las células neuronales. La fase inicial se caracteriza por la aparición de pródromos inespecíficos (cefalea, fiebre, náuseas, vómitos) en 40 a 70% de los pacientes.2 Si bien no es un diagnóstico que se sospeche de primera instancia en los servicios de urgencias, ante la aparición de tres síntomas comunes (fiebre, alteración del estado mental y convulsiones) será conveniente pensar en una punción lumbar.4
La encefalitis autoinmune, asociada con teratomas, se describió por primera vez en 2017.9 Los primeros reportes fueron de mujeres jóvenes, con síntomas psiquiátricos agudos, convulsiones, alteraciones en la memoria, inestabilidad autonómica e hipoventilación central, asociados con teratoma ovárico.
La fisiopatología de los teratomas y la encefalitis no es aún suficientemente conocida. Se ha sugerido que esos tumores están compuestos de las tres capas germinales y en el 96% de los teratomas asociados con encefalitis anti-NMDAR hay tejido nervioso. La expresión ectópica de subunidades NR2 (unido a glutamato) contribuye a romper la tolerancia inmune. Los mecanismos por los que estos anticuerpos traspasan la barrera hematoencefálica son favorecidos por las infecciones.9
La fisiopatología planteada entre encefalitis autoinmune y COVID-19 se divide en una inflamación sistémica, con una tormenta de citocinas, activación de la microglía con daño neurológico secundario y, finalmente, un mimetismo molecular.7
El virus SARS-CoV-2 infecta la célula huésped a través de los receptores de la enzima convertidora de angiotensina 2 (ACE-2) y TMPRSS2 (proteasa transmembrana, serina 2). Las diversas vías de invasión del sistema nervioso central incluyen: transporte axonal retrógrado a través de la mucosa olfatoria, trasmisión transináptica mediante las neuronas infectadas, invasión endotelial, diseminación hematógena directa al sistema nervioso central por medio de los órganos ventriculares, con deficiencia de la barrera hematoencefálica y transporte de virus intracelular a través de células inmunes del huésped infectadas (mecanismo del caballo de Troya). La infección pulmonar por SARS-CoV-2 activa las cascadas inflamatorias, que se acumulan hasta convertirse en una tormenta de citocinas que da lugar a una disfunción endotelial que altera las unidades neurovasculares y provoca la degradación de la barrera hematoencefálica.
Al ingresar al sistema nervioso central, el virus infecta las neuronas vecinas, los oligodendrocitos, los astrocitos y la microglía. La proteína viral S1 hace que la microglía libere una gran cantidad de mediadores inflamatorios, lo que conduce a la activación del receptor ACE-2, HIF-1α (factor 1-α inducible por hipoxia), NOS (óxido nítrico sintasa), P2X7 (activada por ATP) y los receptores purinérgicos (P2), expresión de NLRP-3 (dominio de pirina de la familia NLR que contiene 3) y TNF-α.
Los astrocitos comienzan a funcionar como “centros de replicación” del virus. Se induce una activación de células B vírgenes, que se diferencian en células de memoria y células plasmáticas. Posteriormente, estas células B de memoria ingresan al sistema nervioso central y se reestimulan, con expansión clonal y se diferencian en células plasmáticas, que comienzan a liberar autoanticuerpos contra los antígenos neuronales, células de superficie y objetivos intracelulares. Estos autoanticuerpos, a su vez, interfieren en la trasmisión de señales neuronales y la plasticidad sináptica, que dan lugar a manifestaciones neurológicas.
Las similitudes estructurales de las subunidades NMDAR GluN1 y Glu-N2a con las proteínas no estructurales 8 y 9 del SARS-CoV-2, respectivamente, pueden inducir una reactividad cruzada inmunomediada con el NMDAR. Los complejos de receptores de autoanticuerpos activan, más tarde, las vías posteriores y alteran la célula. Todo ello contribuye a una amplia gama de manifestaciones clínicas.
En la paciente del caso no fue posible conocer si el detonante de la patología nerviosa fue el contagio de SARS-CoV-2 o la aplicación de la vacuna contra el mismo virus. Algunos artículos sí mencionan la relación entre la administración de vacunas y encefalitis. Se informan algunos casos de la relación entre encefalitis autoinmune y las vacunas contra el tétanos, difteria, tosferina, polio y la vacuna H1N1.10,11 Las publicaciones de Hyoung Cheol describen el caso de encefalitis por anticuerpos antirreceptor NMDA después de la vacunación con BNT162b2 m-RNA COVID 19.12 En este artículo se plantea la hipótesis de que los anticuerpos antirreceptor NMDA que coexistían antes de la vacunación podrían activarse con la vacuna. Desde luego que hacen falta más investigaciones para determinar el vínculo preciso entre la vacunación COVID-19 y la encefalitis antirreceptor NMDA.
Por lo que se refiere al tratamiento de esta enfermedad, de acuerdo con la bibliografía consultada, se plantea una guía de tratamiento para la encefalitis por receptor NMDA después de la infección por SARS-CoV-2 (Figura 4) considerando las recomendaciones de expertos internacionales. La primera opción debe ser la inmunosupresión, mediante el tratamiento con corticosteroides (1 g de metilprednisolona al día durante 5 días), administración intravenosa de inmunoglobulina humana (0.4 g/kg/día durante 5 días) o inmunoadsorción o plasmaféresis para la eliminación rápida de autoanticuerpos patógenos. Si el tratamiento falla, deberá ampliarse a los pocos días, de preferencia con rituximab (2 X 1000 mg intravenoso o subcutáneo a intervalos de 2 a 4 semanas). En casos resistentes puede requerirse un tratamiento combinado con ciclofosfamida (750 mg/m2 de superficie corporal cada cuatro semanas), micofenolato de mofetilo o metotrexato para lograr una respuesta clínica. Bortezomib está indicado para el tratamiento escalonado (1 a 6 ciclos de 1.3 mg/m2 de superficie corporal durante 21 días cada ciclo). Además, deben prescribirse antipsicóticos con efectos secundarios extrapiramidales bajos (quetiapina, clozapina) para tratamiento sintomático de los síntomas psicóticos, para reducir el riesgo de discinesia o síndrome neuroléptico maligno inducido por neurolépticos. Las benzodiacepinas de acción corta también están indicadas en ansiolisis, sedación y tratamiento de los síntomas catatónicos.13,14,15

El caso aquí reportado está relacionado con anticuerpos anti-NMDA, aunque estos no siempre se encuentran en pacientes con encefalitis. Las investigaciones de Morooka describen dos casos en los que las pacientes experimentaron síntomas neurológicos, sin anticuerpos anti NMDA, pero sí con el hallazgo de teratomas, cuyos síntomas disminuyeron posterior al tratamiento quirúrgico.10,16
Hoy día, el tratamiento quirúrgico es parte fundamental de la atención médica a estas pacientes. Cuando la paciente del caso tuvo la recidiva del teratoma, posterior al tratamiento quirúrgico preservador de la función, se optó por el procedimiento quirúrgico definitivo, con ooforectomía bilateral. El porcentaje de recidiva de los teratomas se ubica entre 12 y 24% posterior a tratamiento conservador.17 Ante este contexto es relevante individualizar a cada paciente y ofrecer la mejor opción quirúrgica.
Este es el primer caso reportado en México, posterior a la aplicación de vacunas contra COVID-19 y la existencia de teratomas bilaterales.
CONCLUSIONES
Aún no se han determinado todas las enfermedades desencadenadas posterior a la pandemia de la COVID-19: las causadas por el mismo virus y las asociadas con la administración de vacunas. Lo que sí está claro es que se ha incrementado la incidencia de las enfermedades autoinmunes.
Si bien la encefalitis autoinmune no es un diagnóstico frecuente, es importante investigar los antecedentes con relación directa con la enfermedad, como la exposición al virus, entre ellos SARS-CoV-2 y la administración de vacunas. De igual forma, ante la aparición de síntomas neurológicos deben descartarse las tumoraciones, sobre todo de ovario.
Estos cuadros, aunque no tan frecuentes, deben atenderse de manera multidisciplinaria, en conjunto con Medicina interna, Neurología, Radiología e imagen, Ginecología y Obstetricia, Psicología, entre otras, porque el diagnóstico y tratamiento suponen un gran reto para los médicos especialistas.
REFERENCIAS
- Sammim M, Dhar D, Goyal S, Dey T, et al. AI-CoV Study: autoimmune encephalitis associated with COVID-19 and its vaccines. A Systematic review. J Clinical Neurology (Korea) 2022; 692-710. https://doi.org/10.3988/jcn.2022.18.6.692
- Jiménez Ruiz A, Cárdenas Sáenz O, Ruiz Sandoval J. Encefalitis autoinmunitaria secundaria a teratoma ovárico: un nuevo síndrome neuropsiquiátrico. Reporte de caso. Ginecol Obstet Mex 2017; 472-79.
- Titulaer M, McCracken L, Gabilondo I. Treatment and prognostic factors for long-term outcome in patients with anti-NMDA receptor encephalitis: an observational cohort study. Lancet Neurology 2013; 157-165.
- Gong X, Chen C, Liu X. Long-term functional outcomes and relapse of anti-NMDA receptor encephalitis: a cohort study in Western China. Neurology Neuroimmunology & Neuroinflammation 2021; 8. https://doi.org/ 10.1212/NXI.0000000000000958
- Wang H. Anti-NMDA receptor encephalitis and vaccination. Int J Molecular Sciences 2017; 18: 193. https://doi.org/10.3390/ijms18010193
- Hofmann C, Baur M, Schroten H. Anti-NMDA receptor encephalitis after TdaP-IPV booster vaccination: cause or coincidence? J Neurology 2011; 258:500-1. https://doi.org/10.1007/s00415-010-5757-3
- Hyoung Cheol L, Byung-Kun K, Kyusik K, Woong-Woo L, et al. Anti-N-Methyl-D-aspartate receptor encephalitis after BNT162b2 COVID-19 vaccination. J Epilepsy Research 2022; 12: 71-73. https://pmc.ncbi.nlm.nih.gov/articles/PMC9830031/
- Nguyen L, Wang C. Anti-NMDA receptor autoinmune encephalitis: diagnosis and management strategies. Int J General Medicine 2023; 7-21. https://doi.org/10.2147/IJGM.S397429
- Dalmau J, Tuzun E, Wu H, Masjuan J, et al. Paraneoplatic anti-N-methyl-D-aspartate receptor encephalitis associated with ovarian teratoma. Annales de Neurología 2007; 61: 25-36. https://doi.org/10.1002/ana.21050
- Morooka M, Hiraga A, Tanaka K, Yoshizaki S, et al. Two cases of encephalitis without anti-N-methyl-D-aspartate receptor antibody successfully treated with ovarian teratoma resection and immunotherapy. Int Med Jap S Internal Medicine 2023; 1817-20. https://doi.org/10.2169/internalmedicine.0447-22
- Barry H, Byrne S, Barret E, Murphy KC, et al. Anti-N-methyl-D-aspartate receptor encephalitis: review of clinical presentation, diagnosis and treatment. BJPsych Bull 2015; 39 (1):19-23. https://doi.org/10.1192/pb.bp.113.045518
- Xu J, Zhao N, Guan H, Walline JH, et al. Anti-N-methyl-D-aspartate receptor encephalitis: characteristics and rapid diagnostic approach in the emergency department. BMC Neurology 2022; 22:224. https://doi.org/10.1186/s12883-022-02752-9
- Davis A. COVID evaluation model estimates 57 percent of world population infected at least once 2022. https://www.newsweek.com/covid-evaluation-model-estimates-57-percent-world-population-infected-least-once-1672440
- Lynch D, Ratelle A, Na YD, Rosling K, et al. Anti-NMDA receptor encephalitis: clinical features and basic mechanisms. Advances in Pharmacology 2017; 82, 235-60. https://doi.org/10.1016/bs.apha.2017.08.005
- Steiner J, Prüss H, Köhler S, Frodi T, et al. Autoimmune encephalitis with psychosis: Warning signs, step-by-step diagnostics and treatment. World J Biol Psychiatry 2020; 21 (4): 241-54. https://doi.org/10.1080/15622975.2018.1555376
- Dalmau J, Armangué T, Planagumà J, Radosevic M, et al. An update on anti-NMDA receptor encephalitis for neurologists and psychiatrists: mechanisms and models. Lancet Neurology 2019; 8 (11): 1045-105. https://doi.org/10.1016/S1474-4422(19)30244-3
- Graus F, Titulaer M, Balu R, Benseler S, et al. A clinical approach to diagnosis of autoinmune encephalitis. Lancet Neurology 2016; 15 (4): 391-404. https://doi.org/10.1016/S1474-4422(15)00401-9