RESUMEN
ANTECEDENTES: La leucemia aguda pocas veces se manifiesta durante el embarazo, lo que hace que sea inusual recurrir a un método diagnóstico para descartar cualquier leucemia.
CASO CLÍNICO: Paciente de 26 años, con antecedentes de un embarazo y una cesárea, con ingreso al hospital a las 37.5 semanas de la gestación actual, con diagnóstico de preeclampsia aguda y trombocitopenia por lo que se decidió la finalización del embarazo mediante cesárea. Con base en los parámetros de laboratorio se confirmó el puerperio quirúrgico patológico, preeclampsia y síndrome de HELLP Mississippi 1. Tres días después del procedimiento quirúrgico los estudios de laboratorio se reportaron con múltiples alteraciones que ameritaron su traslado a un centro de tercer nivel de atención en donde se estableció el diagnóstico de trombocitopenia y leucemia linfoblástica aguda tratada con quimioterapia, con resistencia al primer esquema y sin respuesta al segundo que derivó en el fallecimiento de la paciente.
PALABRAS CLAVE: Leucemia mieloide aguda, embarazo, preeclampsia, trombocitopenia, síndrome HELLP, diagnóstico diferencial, diagnóstico tardío, anomalías múltiples
ABSTRACT
BACKGROUND: Acute leukemia rarely manifests during pregnancy, so it is uncommon to use diagnostic methods to rule out leukemia.
CLINICAL CASE: A 26-year-old patient with a history of one pregnancy and a C-section was admitted at 37.5 weeks with a diagnosis of acute preeclampsia and thrombocytopenia. It was decided to terminate the pregnancy via C-section. Based on laboratory parameters, pathological surgical puerperium, preeclampsia, and HELLP (hemolysis, elevated liver enzymes, low platelets) syndrome were confirmed. Three days after the procedure, laboratory tests revealed multiple abnormalities, prompting her transfer to a tertiary care center. There, she was diagnosed with thrombocytopenia and acute lymphoblastic leukemia. She was treated with chemotherapy, but was resistant to the first regimen and did not respond to the second, ultimately leading to her death.
KEYWORDS: Leukemia myeloid acute, Pregnancy, Preeclampsia, Thrombocytopenia, HELLP syndrome, Diagnosis differential, Delayed diagnosis, Abnormalities multiple
ANTECEDENTES
La preeclampsia y la eclampsia afectan del 2 al 8% de las embarazadas.1 En el ámbito internacional ambas se ubican en el tercer lugar de la mortalidad materna.2 El síndrome HELLP es una complicación de los trastornos hipertensivos del embarazo en pacientes con preeclampsia y eclampsia.3
La preeclampsia grave puede manifestarse con tensión arterial normal o sin proteinuria, como ocurre en el 10 al 20% de los casos de síndrome HELLP.3,4 Para establecer el diagnóstico de síndrome HELLP se requiere, primero, identificar algún trastorno hipertensivo del embarazo y, posteriormente, la triada de hemólisis, elevación de enzimas hepáticas y trombocitopenia.5
Estos trastornos deben distinguirse de otros padecimientos infrecuentes, como la leucemia mieloide y linfoblástica, con incidencia en el embarazo de 1 caso por cada 75,000 a 100,000 gestaciones.6-8
Las alteraciones en los recuentos sanguíneos periféricos, como la anemia y la trombocitopenia, pueden interpretarse erróneamente como síntomas relacionados con el embarazo, lo que lleva a un diagnóstico tardío y a un tratamiento inadecuado.6,7
CASO CLÍNICO
Paciente de 26 años, con antecedentes de un embarazo y una cesárea (a los 19 años) esta última indicada por cumplimiento de 41 semanas de gestación, carencia de progresión del trabajo de parto pero con recién nacido sano. Ingresó al Hospital de la Mujer de Culiacán, referida del Hospital General de Guasave, Sinaloa, debido a trombocitopenia aguda de 10,000 plaquetas por μL y deshidrogenasa láctica de 2,000 UI/L, con cifras tensionales normales, 110-72 mmHg y con 37.5 semanas de la gestación actual. Al ingreso a urgencias se encontró asintomática y sin signos de vasoespasmo. El ultrasonido obstétrico reveló la existencia de un feto único en posición longitudinal, presentación cefálica, frecuencia cardiaca de 145 lpm y peso fetal estimado de 4171 g.
La paciente tenía un control prenatal presuntivo adecuado con siete consultas en su centro de salud. Se encontraba consciente y orientada, sin afectación cardiopulmonar. Con abdomen distendido debido al embarazo. En el examen ginecológico el cuello uterino posterior se advirtió cerrado, con reflejos osteotendinosos normales y sin edema en las extremidades. La presión arterial al ingreso fue de 147-85 mmHg. En el análisis sanguíneo preoperatorio la paciente reportó: hemoglobina (Hb) 11.5 g/dL, plaquetas 11,000/mm, leucocitos 17.4 x 10/UL, aspartato aminotransferasa 57.2 UI/L, alanino aminotransferasa (ALT) 21.2 UI/L, LDH 3,698 UI/L, glucosa 131 mg/dL, creatinina 0.7 mg/dL, pruebas antidengue negativas y sin otras anormalidades.
Se determinó que se encontraba en las 37.5 semanas de embarazo, con diagnóstico de preeclampsia aguda, con trombocitopenia. La paciente otorgó su consentimiento informado, por escrito, para la evacuación uterina quirúrgica. Se decidió la cesárea, tipo Kerr, previa transfusión de dos concentrados de plaquetas al ingreso, dos más antes de la cirugía y dos más durante el transoperatorio. Se obtuvo una recién nacida de 3190 g, talla de 50 cm, Apgar 8-9 y Silverman de 01, con adecuada evolución clínica y dada de alta con lactancia materna exclusiva.
Posterior a la cesárea, la paciente se trasladó a la unidad de cuidados intensivos con tensión arterial de 154-84 mmHg, y los siguientes parámetros analíticos: Hb 8.4 g/dL, plaquetas 21,000/mm, leucocitos 17 x 10^3/UL, glucosa 97 mg/dL, creatinina 0.5 mg/dL, LDH 2,705 UI/L, lo que confirmó un puerperio quirúrgico patológico, preeclampsia y síndrome HELLP Mississippi 1. Se le indicó tratamiento con 30 mg de nifedipino cada 8 h y 100 mg metoprolol cada 12 h, ambos por vía oral. Además, 8 mg de dexametasona intravenosa cada 12 h y 1 g de sulfato de magnesio cada 24 h. Más transfusión de plaquetas por aféresis.
Durante su permanencia en cuidados intensivos la tensión arterial permaneció en 120-130/80 mmHg, con mejoría de la función hepática y disminución de las concentraciones de LDH. La recolección de proteínas en orina fue de 669.0 mg/24 h. Sin embargo, tres días después del procedimiento quirúrgico, el hemograma reportó trombocitopenia persistente de 21,000/mm, por lo que se aumentó la dosis de dexametasona a 40 mg por vía intravenosa cada 24 h y se redujo el metoprolol a 50 mg por vía oral cada 12 h para mantener la presión arterial en límites objetivo. Continuó en seguimiento fuera de la unidad de cuidados intensivos.
Después de siete días de hospitalización en el servicio de obstetricia, el examen de sangre reportó Hb 10.3 g/dL, plaquetas 54,000/mm, leucocitos 9.8 x 10^3/UL, glucosa 97 mg/dL, creatinina 0.6 mg/dL, AST 22.8 UI/L, ALT 29.6 UI/L y LDH 1,676 UI/L; con un evidente aumento de plaquetas pero con función aún en riesgo debido al bajo conteo y concentraciones elevadas de LDH. Figura 1
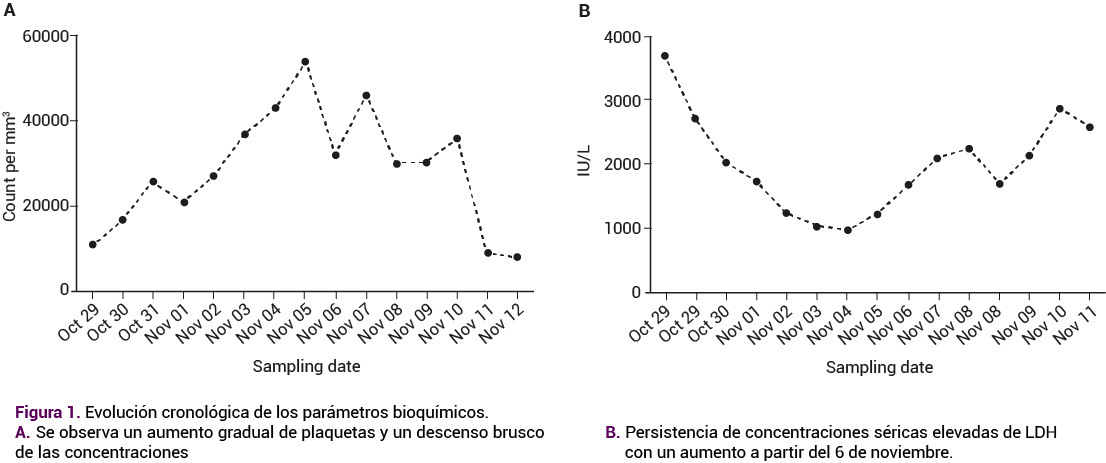
Por lo anterior, la paciente se trasladó al servicio de hematología del Hospital General Regional 1 del Instituto Mexicano del Seguro Social (IMSS), donde finalmente se estableció el diagnóstico de trombocitopenia y leucemia linfoblástica aguda de células B L2 por la clasificación Franco Americana Británica (FAB), mediante inmunofenotipificación de médula ósea, por lo que se indicó el protocolo Berlin-Frankfurt-Munster 95 (BFM-95) fase A. Debido a la resistencia al tratamiento previo se optó por la quimioterapia con fludarabina, citarabina, factor estimulante de colonias de granulocitos e idarubicina (FLAG-IDA).
Posteriormente, el riesgo molecular reveló el cromosoma Filadelfia por la positividad a la fusión del gen proteína de la región de punto de ruptura (BCR) en el cromosoma 22 y tirosina-proteína cinasa 1 (ABL1) en el cromosoma 9 (BCR::ABL), por lo que se le indicó un inhibidor de la tirosina cinasa (TKI), imatinib, con la que experimentó una evolución adversa con citopenias profundas. El tratamiento se reemplazó con dasatinib, otro inhibidor de la tirosina cinasa. El tratamiento de quimioterapia establecido más la gravedad de la leucemia derivaron en la muerte de la paciente al séptimo mes del diagnóstico.
DISCUSIÓN
El acrónimo síndrome HELLP hace referencia a las características bioquímicas que lo definen: hemólisis, enzimas hepáticas elevadas y plaquetas bajas.5 La hemólisis se caracteriza por alteraciones en la morfología de los glóbulos rojos documentadas en frotis de sangre periférica (esquistocitos, agregación plaquetaria, células diana, etc.), elevación de LDH sérica ≥ 600 U/L, bilirrubina total ≥ 1.2 mg/dL, disminución de la hemoglobina, el hematocrito y de la haptoglobina sérica.5 Por otro lado, la elevación de las enzimas hepáticas se indica por AST ≥ 70 U/L, ALT ≥ 50 U/L y LDH sérica ≥ 600 U/L.5
Si bien el síndrome HELLP se considera un subtipo de preeclampsia grave, en realidad es un padecimiento diferente. Esto se evidencia por el hecho de que el 20% de las pacientes embarazadas con diagnóstico de síndrome HELLP carecen de antecedentes de tensión arterial elevada o proteinuria.9 La causa del síndrome HELLP no está del todo clara; se ha sugerido que los cambios inmunológicos, la agregación de plaquetas, la disfunción endotelial, la presión arterial elevada y el error innato del metabolismo oxidativo de los ácidos grasos son factores etiológicos potenciales.10 Además, los estudios han mostrado concentraciones elevadas de factores antiangiogénicos (sFlt-1 y sEng) y disminuidas de mediadores proangiogénicos (PIGF) en mujeres embarazadas con síndrome HELLP.11
De acuerdo con las características clínicas del síndrome HELLP, la clasificación de Mississippi divide la enfermedad en tres clases según el recuento de plaquetas en sangre: Clase I: trombocitopenia grave (menos de 50,000 plaquetas por mm3), Clase II: trombocitopenia moderada (entre 50,000 y 100,000 plaquetas por mm3) y Clase III: trombocitopenia leve (más de 100,000 plaquetas por mm3). Esta clasificación ayuda a predecir la gravedad del cuadro clínico y el riesgo de complicaciones posparto.12
Durante el embarazo, los recuentos sanguíneos periféricos, como la anemia y la trombocitopenia, pueden interpretarse como síntomas relacionados con el embarazo, lo que lleva a un diagnóstico tardío y un tratamiento inadecuado.13 Es importante establecer el diagnóstico diferencial correcto porque las causas potencialmente responsables pueden incluir afecciones graves, como el síndrome HELLP, la púrpura trombocitopénica inmunitaria o las neoplasias hematológicas.13
Si bien también puede haber tumores en mujeres en edad fértil, los que aparecen en este límite de edad, en orden de frecuencia son: cáncer de mama, de cuello uterino y los tumores hematológicos.14,15 En esta última categoría, la leucemia linfoblástica aguda es una enfermedad hematológica maligna que surge de las células mieloides o linfoides. La incidencia aumenta de manera importante con la edad y alcanza su punto máximo entre los 80 y 85 años. La incidencia de leucemia en el embarazo es de 1 caso por cada 75,000 a 100,000 gestaciones,7,8,13 aunque recientemente se han informado incidencias superiores a 1 en 10,000.16
Las leucemias mieloides son consecuencia de la transformación neoplásica de las células precursoras hematopoyéticas, caracterizada por la proliferación de células precursoras inmaduras o blastos en la médula ósea, lo que da lugar a citopenias que incluyen anemia, neutropenia y trombocitopenia.17,18 Además, las leucemias mieloides tienen una tasa de incidencia de 1 a 2 por cada 100,000 embarazadas, de las que la leucemia mieloide aguda representa aproximadamente dos tercios y la leucemia linfoblástica aguda alrededor de un tercio.17,18 Casi dos tercios de las leucemias en pacientes embarazadas son mieloides y su diagnóstico se establece en el segundo (37%) y tercer trimestre (40%) de la gestación.19
El aumento en las concentraciones de LDH y la disminución de la trombocitopenia en la paciente hicieron sospechar una causa alternativa; por eso se envió al servicio de Hematología del IMSS para una valoración hematológica integral mediante inmunofenotipificación de médula ósea y estudio de riesgo molecular.20 Cuando el diagnóstico se establece después de las 32 semanas de embarazo, podría ser razonable finalizarlo antes de iniciar la quimioterapia. Hoy en día las tasas de remisión reportadas en estas pacientes son del 70 al 75%.20,21 Lo lamentable es que, a pesar del tratamiento de quimioterapia, la gravedad de la manifestación leucémica empeoró las condiciones de salud de la paciente, que derivaron en la muerte.21
Se obtuvo el consentimiento informado de la madre para la publicación de este artículo. La familia de la paciente expresó su agradecimiento por el trato recibido desde su ingreso al triage, la atención recibida y el buen trato de los pediatras hacia su recién nacido.20
CONCLUSION
Si bien el inicio tardío del tratamiento de quimioterapia suele asociarse con mal desenlace para la madre, retrasarlo para permitir primero el parto puede ser razonable en pacientes con diagnóstico tardío, más allá de las 30 semanas de embarazo; este retraso tiene como propósito minimizar la exposición del feto a la quimioterapia. Es fundamental considerar una amplia gama de diagnósticos diferenciales, manifestaciones clínicas durante el embarazo y tratamiento conforme a las pautas establecidas.
AGRADECIMIENTOS
Agradecemos todas las facilidades otorgadas por el Hospital de la Mujer y el Instituto Mexicano del Seguro Social, al equipo de médicos cirujanos, pediatras y paramédicos para la atención brindada a la madre y al recién nacido.
REFERENCIAS
- Gestational Hypertension and Preeclampsia: ACOG Practice Bulletin, Number 222. Obstetrics & Gynecology 2020; 135 (6): e237-e60. https://doi.org/10.1097/aog.0000000000003891
- Organization WH. Trends in maternal mortality 2000 to 2023: estimates by WHO, UNICEF, UNFPA, World Bank Group and UNDESA/Population Division, 2025. https://www.who.int/publications/i/item/9789240108462
- Arigita Lastra M, Martínez Fernández GS. [HELLP syndrome: controversies and prognosis]. Hipertens Riesgo Vasc 2020; 37 (4): 147-51. https://doi.org/10.1016/j.hipert.2020.07.002
- Karumanchi SA, Maynard SE, Stillman IE, et al. Preeclampsia: a renal perspective. Kidney Int 2005; 67 (6): 2101-13. https://doi.org/10.1111/j.1523-1755.2005.00316.x
- Vigil-De Gracia P. Síndrome HELLP. Ginecol Obstet Mex 2015; 83 (1). https://ginecologiayobstetricia.org.mx/articulo/sindrome-hellp
- Ali R, Ozkalemkaş F, Ozçelik T, et al. Maternal and fetal outcomes in pregnancy complicated with acute leukemia: a single institutional experience with 10 pregnancies at 16 years. Leuk Res 2003; 27 (5): 381-5. https://doi.org/10.1016/S0145-2126(02)00182-0
- McGregor AK, Das-Gupta E. Acute myeloid leukaemia in pregnancy. Br J Haematol 2015; 170 (4): 441-2. https://doi.org/10.1111/bjh.13550
- Abadi U, Koren G, Lishner M. Leukemia and lymphoma in pregnancy. Hematol Oncol Clin North Am 2011; 25 (2): 277-91, vii. https://doi.org/10.1016/j.hoc.2011.01.001
- Liu Q, Ling GJ, Zhang SQ, et al. Effect of HELLP syndrome on acute kidney injury in pregnancy and pregnancy outcomes: a systematic review and meta-analysis. BMC Pregnancy Childbirth 2020; 20 (1): 657. https://doi.org/10.1186/s12884-020-03346-4
- Yildirim G, Gungorduk K, Gul A, et al. HELLP Syndrome: 8 Years of Experience from a Tertiary Referral Center in Western Turkey. Hypertension in Pregnancy 2012; 31 (3): 316-26. https://doi.org/10.3109/10641955.2010.507849
- Joshi D, James A, Quaglia A, et al. Liver disease in pregnancy. Lancet 2010; 375 (9714): 594-605. https://doi.org/10.1016/S0140-6736(09)61495-1
- Khalid F, Mahendraker N, Tonismae T. HELLP Syndrome. StatPearls. Treasure Island (FL): StatPearls Publishing; 2025. https://www.ncbi.nlm.nih.gov/books/NBK560615/
- Zhu D, Tang D, Chai X, et al. Acute leukemia in pregnancy: a single institutional experience with 21 cases at 10 years and a review of the literature. Ann Med 2021; 53 (1): 567-75. https://doi.org/10.1080/07853890.2021.1908586
- Ali S, Jones GL, Culligan DJ, et al. Guidelines for the diagnosis and management of acute myeloid leukaemia in pregnancy. Br J Haematol 2015; 170 (4): 487-95. https://doi.org/10.1111/bjh.13554
- Sanz MA, Montesinos P, Casale MF, et al. Maternal and fetal outcomes in pregnant women with acute promyelocytic leukemia. Ann Hematol 2015; 94 (8): 1357-61. https://doi.org/10.1007/s00277-015-2372-5
- Milojkovic D, Apperley JF. How I treat leukemia during pregnancy. Blood 2014; 123 (7): 974-84. https://doi.org/10.1182/blood-2013-08-283580
- Fracchiolla NS, Sciumè M, Dambrosi F, et al. Acute myeloid leukemia and pregnancy: clinical experience from a single center and a review of the literature. BMC Cancer 2017; 17 (1): 442. https://doi.org/10.1186/s12885-017-3436-9
- Nolan S, Czuzoj-Shulman N, Abenhaim HA. Obstetrical and newborn outcomes among women with acute leukemias in pregnancy: a population-based study. J Matern Fetal Neonatal Med 2020; 33 (20): 3514-20. https://doi.org/10.1080/14767058.2019.1579188
- Oduncu FS, Kimmig R, Hepp H, et al. Cancer in pregnancy: maternal-fetal conflict. J Cancer Res Clin Oncol 2003; 129 (3): 133-46. https://doi.org/10.1007/s00432-002-0406-6
- Patel SJ, Ajebo G, Kota V, et al. Analysis of outcomes in hospitalized pregnant patients with acute myeloid leukemia. Am J Blood Res 2020; 10 (4): 68-75. https://pmc.ncbi.nlm.nih.gov/articles/PMC7486487/pdf/ajbr0010-0068.pdf
- Avivi I, Brenner B. Management of acute myeloid leukemia during pregnancy. Future Oncol 2014; 10 (8): 1407-15. https://doi.org/10.2217/fon.14.641