RESUMEN
ANTECEDENTES: El hecho de que algunos implantes de varilla sean radioopacos facilita su localización cuando migran.
CASO CLÍNICO: Paciente de 25 años, con antecedente de un embarazo y un parto; además, un implante subdérmico de etonogestrel. Acudió a consulta para el retiro del implante, luego de tres años de uso; sin embargo, la extracción fue fallida, pues no se logró su palpación. En la radiografía de tórax, en el parénquima pulmonar, se advirtió una imagen hiperintensa. Se solicitó la valoración del cirujano vascular, quien indicó y efectuó el procedimiento quirúrgico para la extracción, con cateterismo cardiaco derecho y un mini catéter para extracción del implante, de 2 a 4 mm y de 17.5 cm de largo. La intervención fue exitosa y transcurrió sin contratiempos.
CONCLUSIÓN: Cuando el dispositivo subdérmico implantado no es palpable debe pensarse no solo en una implantación profunda sino en la migración a distancia o embolización de la arteria pulmonar. Por sus características radioopacas los implantes pueden detectarse con el auxilio de medios de imagen avanzados, ubicarlos y extraerlos.
PALABRAS CLAVE: Migración pulmonar, embarazo, etonogestrel, parénquima pulmonar, cirujano vascular, cateterismo cardiaco derecho, arteria pulmonar
ABSTRACT
BACKGROUND: The fact that some rod implants are radio-opaque makes it easier to locate them when they migrate.
CLINICAL CASE: 25-year-old female patient with a history of pregnancy and childbirth and a subdermal etonogestrel implant. She presented to the clinic for removal of the implant after three years of use; however, the extraction was unsuccessful as it could not be palpated. The chest x-ray revealed a hyperintense lung parenchyma. The vascular surgeon was asked to evaluate the situation, and he ordered and performed the surgical procedure for extraction with right heart catheterization and a miniature implant extraction catheter, 2 to 4 mm and 17.5 cm long. The operation was successful and uneventful.
CONCLUSION: If the implanted subdermal device is not palpable, not only deep implantation but also migration to a distant site or embolization of the pulmonary artery should be considered. Because of their radio-opaque properties, the implants can be detected, localized, and removed using advanced imaging techniques.
KEYWORDS: Lung migration, Pregnancy, Etonogestrel, Lung parenchyma, Vascular surgeon, Right heart catheterization
ANTECEDENTES
Algunos implantes subdérmicos pueden, ocasionalmente, por sus características radioopacas, ser difíciles de localizar, incluso mediante técnicas de imagen avanzadas.1 Cuando se ubican fuera del área de colocación, lo hacen a sitios diferentes, incluso al sistema arterial pulmonar.2
El implante de etonogestrel proporciona un efecto anticonceptivo con alcance hasta de tres años. Contiene 15 mg de sulfato de bario (lo que lo hace radioopaco) para permitir su visualización con métodos de imagen.3 Es una varilla de 4 cm de longitud y 2 mm de diámetro que se coloca entre 8 y 10 cm por encima del cóndilo lateral interno del codo, en la cara medial del brazo no dominante.4
En algunas ocasiones, los implantes se colocan sin seguir el procedimiento y técnica descrita por el fabricante; en consecuencia, no siempre es fácil ubicarlos por medio de la palpación, otras veces se dejan en sitios incorrectos que requieren técnicas complejas para su retiro.5
Cuando en algunas pacientes la radiografía de tórax y la tomografía computada no logran localizar el implante se recurre a la ecografía de alta frecuencia y resonancia magnética del brazo.6,7
Los implantes están diseñados para detectarse mediante palpación directa en el brazo donde se colocan; sin embargo, en raras ocasiones embolizan. Se ha descrito un probable recorrido desde una vena grande, cercana al sitio de inserción, con recorrido hacia la aurícula o ventrículo derechos hasta alcanzar la vasculatura pulmonar.7 Las pacientes deciden recibir y retirar el dispositivo en distintas etapas de la vida y por múltiples razones.7 La mayoría son pacientes jóvenes, sin comorbilidades.7 Cuando estos dispositivos migran, la paciente puede volverse, de un momento a otro o gradualmente sintomática o permanecer asintomática. O, bien, sospechar la migración cuando no se percibe el dispositivo por palpación.8,9
A partir del año 2011, los servicios de Planificación Familiar y de Radiología del Hospital General de México colaboran con otros servicios de planificación familiar del área metropolitana en la ubicación y retiro de implantes de difícil localización.3,4
Los efectos secundarios del uso prolongado de los implantes de etonogestrel se han investigado ampliamente, sobre todo los relacionados con empeoramiento de la función sexual, con disminución de la globulina fijadora de hormonas sexuales (SHBG), con potencial efecto negativo en la calidad de vida de las usuarias.10
CASO CLÍNICO
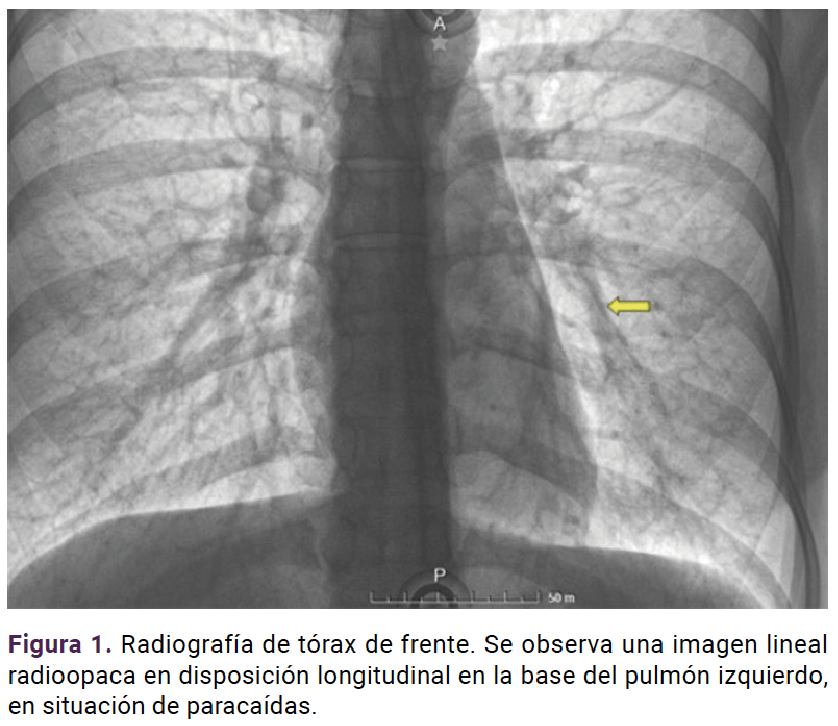
Paciente de 25 años, con menarquia a los 13 años, e inicio de la vida sexual activa a los 18 años, dismenorrea, ciclos irregulares, un embarazo, un parto y aplicación posparto de un implante subdérmico de etonogestrel. Tres años después de la colocación acudió a la unidad de planificación familiar para el retiro del implante, con extracción fallida (no se logró palparlo). Se practicaron estudios de imagen complementarios para su ubicación, entre ellos una radiografía de tórax (Figura 1) en la que se visualizó una imagen hiperintensa en el área del parénquima pulmonar.
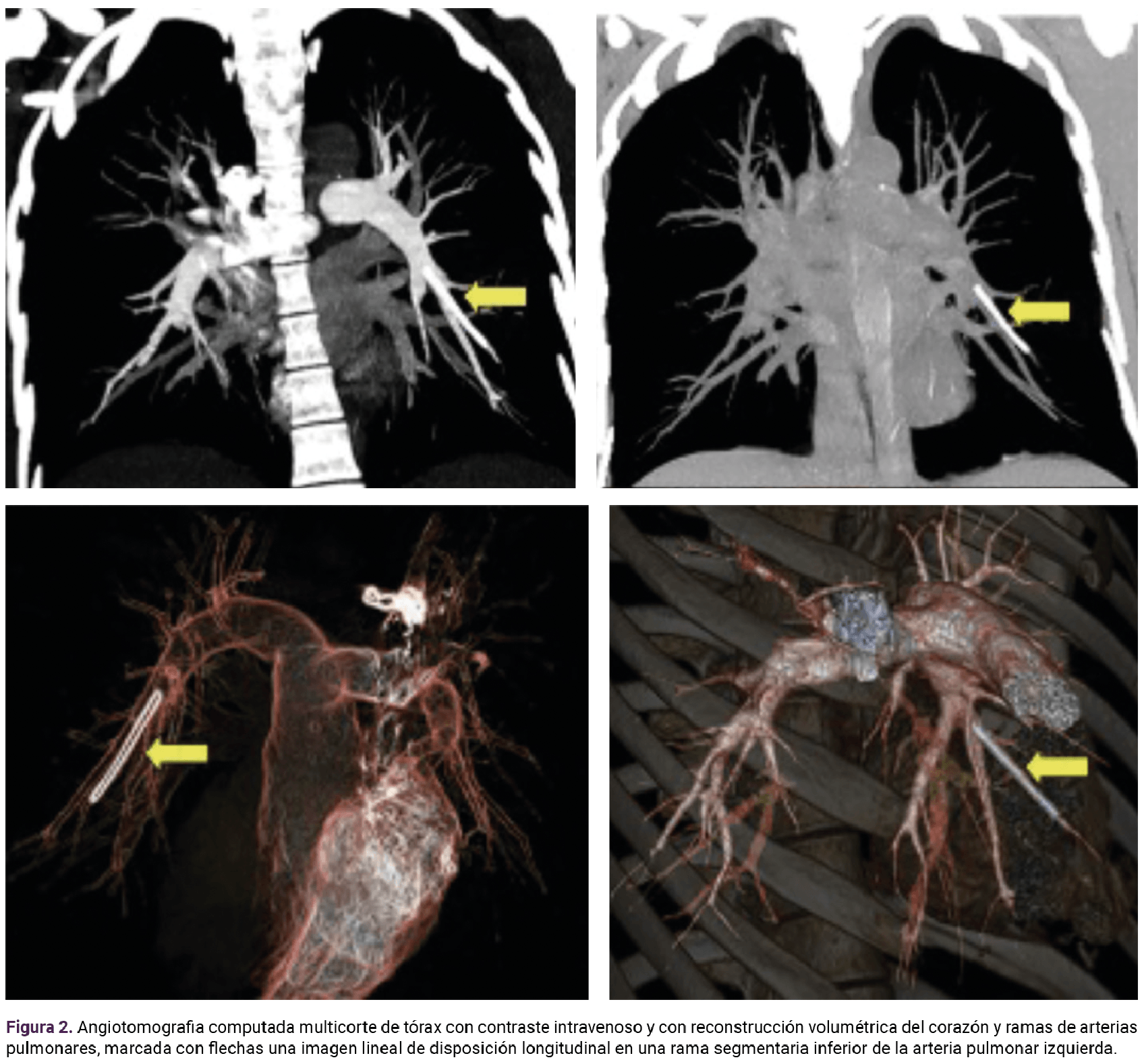
En la valoración integral de la paciente se advirtieron indicios de dificultad respiratoria, con polipnea al momento de esfuerzos físicos de pequeña intensidad. La angiotomografia computada de las arterias pulmonares, indicada por la imagen sugerente de implante subdérmico en torno del parénquima pulmonar y que se corroboró en la rama de la arteria pulmonar izquierda. Figura 2
En la valoración por parte del cirujano vascular se indicó el tratamiento quirúrgico que permitira la extracción del implante. Se le aplicó un cateterismo cardiaco derecho y un mini catéter para extracción de 2-4 mm y de 17.5 cm de largo. Figura 3

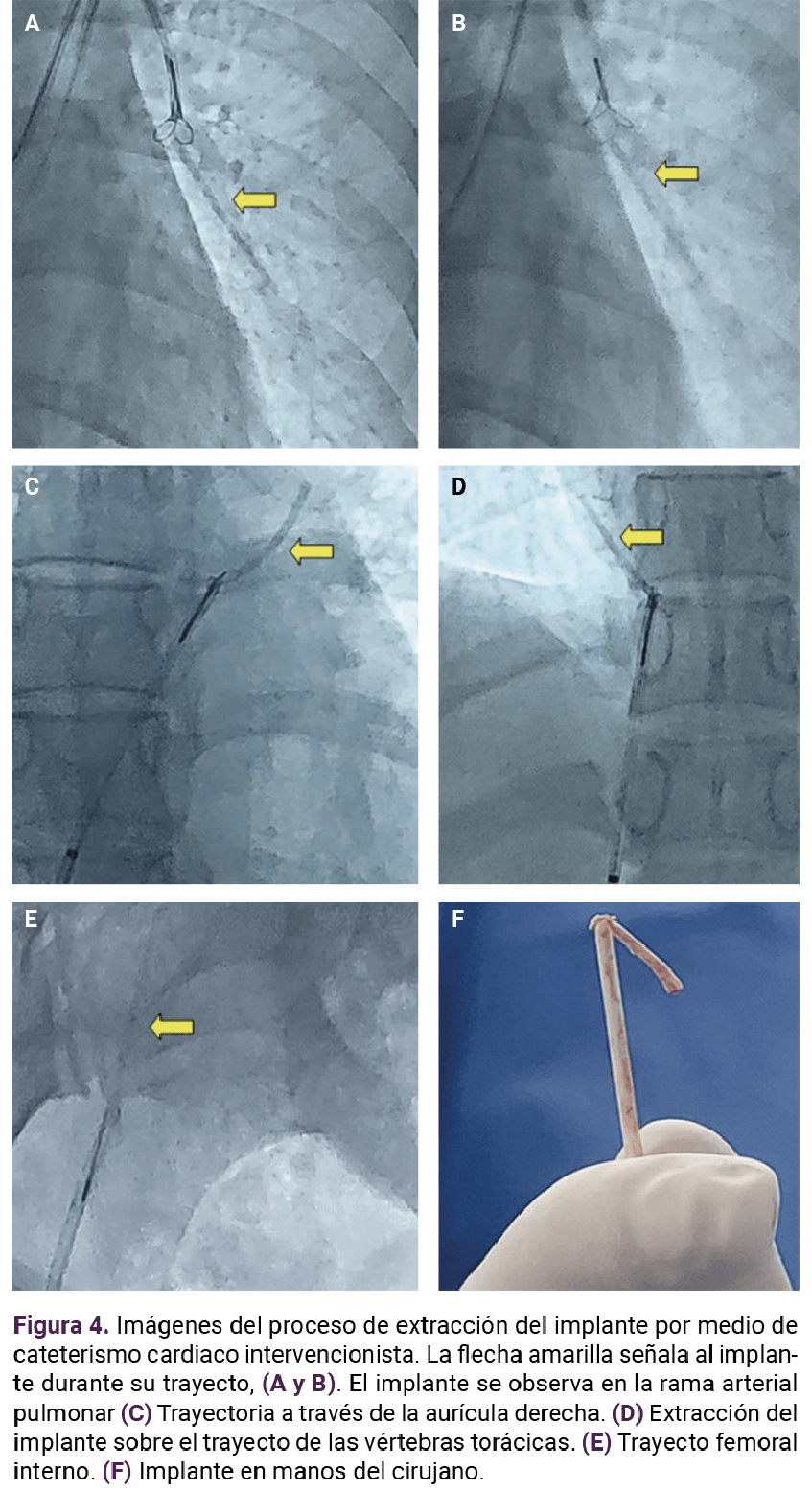
El procedimiento quirúrgico transcurrió sin contratiempos, con la extracción del implante de etonogestrel (Figura 4). La fluoroscopia en tiempo real que evidenció la integridad vascular. La evolución posoperatoria fue favorable y luego del alta hospitalaria ha tenido valoraciones periódicas en la consulta externa sin reporte de alteraciones o molestias.
DISCUSIÓN
La incidencia estimada de migración del implante de etonogestrel a la vasculatura pulmonar se ha descrito en 3.17 por cada 100,000 implantes.10,11 La migración de alto grado (definida como un desplazamiento mayor de 2 cm) es poco frecuente.11 La estadística descrita por la Encuesta Nacional de Crecimiento Familiar estimó que el 5.6% de las mujeres de entre los 15 a 49 años utilizan implantes anticonceptivos (n = 5594), y de 5.8 del 2017 al 2019 (n = 6141).11,12 Aún no se ha encontrado alguna explicación razonable del porqué de la migración del implante subdérmico. Una posible explicación es una técnica de inserción defectuosa, por inexperiencia, a demasiada profundidad o al avanzar el introductor.16
Está descrito que una implantación profunda, y no la migración, es la causa de gran parte de los casos no palpables.12 Otra causa teórica descrita es el cambio rápido en el peso corporal entre el tiempo de la colocación y el de extracción, o una actividad extenuante.13 Una pérdida sustancial de peso posterior a la inserción del dispositivo puede provocar una reducción del soporte por parte de los tejidos circundantes, con aumento de la probabilidad de migración cráneocaudal.13
Enseguida de la colocación del implante debe enseñársele a la paciente a palpar el dispositivo, para que en cualquier momento pueda localizarse.13 Además, que ante cualquier irregularidad al respecto acudan de inmediato a la consulta médica.14
La radiopacidad de estos dispositivos permite su identificación mediante radiografías simples. Al no percibirse por palpación se indica una radiografía de brazo, que en caso de no ser concluyente el siguiente paso es una radiografía de tórax. Si hubiera alguna alteración proceder a la tomografía computada para una localización más precisa.14
Si la paciente desea la extracción del implante, o si se encuentra sintomática a causa del dispositivo, debe considerarse un procedimiento mínimamente invasivo, como la extracción endovascular. La ventaja de ésta es la conservación del tejido pulmonar y evitar el dolor de las incisiones en la pared torácica. Desde luego que siempre es posible que se dificulte la extracción por la tendencia del implante a encapsularse y adherirse al tejido adyacente. Si bien el encapsulamiento tiene como propósito impedir que el implante abandone su lugar de colocación primario, ello puede resultar problemático si sobreviene luego de que el dispositivo se ha desplazado.14,15
De los casos notificados de migración de un dispositivo anticonceptivo desde la parte superior del brazo a la vasculatura pulmonar puede considerarse la extracción endovascular por un médico intervencionista, como en la paciente del caso, lo que disminuye la necesidad de un procedimiento abierto, con mayor morbilidad y riesgo de complicaciones.14,15
Están descritos 55 casos en los que se reporta la embolización del implante anticonceptivo, con una recuperación exitosa de 21 de los casos sin complicaciones relevantes.14 La sospecha de migración es muy variada, algunas pacientes pueden permanecer asintomáticas, con signos de embolia pulmonar en caso de migración del implante, hasta la lesión de un lóbulo pulmonar que requerirá de su extracción.15 Existen pocos estudios en los que se correlacione el tiempo transcurrido desde la implantación con el éxito de la extracción endovascular.15,16
CONCLUSIÓN
Cuando el dispositivo anticonceptivo subdérmico implantado no es palpable, el clínico debe considerar la posibilidad no solo de implantación profunda sino también de migración a distancia o embolización de la arteria pulmonar.
Por sus características radiopacas, el implante puede detectarse mediante radiografía intervencionista, lo que hace más fácil su localización y extracción. La técnica de colocación del dispositivo es en realidad lo más importante; debe evitarse el surco entre el bíceps y el tríceps, por donde discurren las venas basílica y sus ramas.
La palpación y visualización del médico y la paciente inmediatamente después de colorcar el implante y su apropiada documentación evidenciada en la nota clínica y una radiografía como parte del protocolo de correcta localización e inserción del implante permitirán la pronta localización si deja de ser palpable.
REFERENCIAS
- Akhtar MM, Bhan A, Lim Z, Akhtar MA, et al. Percutaneous extraction of an embolized progesterone contraceptive implant from the pulmonary artery. J Contracept 2018; 9: 57-61. https://doi.org/10.2147/oajc.s165827
- Barlow-Evans R, Jaffer K, Balogun M. Migration of a Nexplanon contraceptive implant to the pulmonary artery. BMJ Case Reports 2017: 219259. https://doi.org/10.1136/bcr-2017-219259
- Buitron R, Rodriguez A, Gonzalez J, Vargas A, et al. P711 Complex location of subdermic single-rod contraceptive implant: A case report. Int J Gynaecol Obstet 2009: 107 (S2), S616. https://doi.org/10.1016/s0020-7292(09)62202-5
- Buitrón-García FR, Oropeza-Rechy G, González-de la Cruz J, Lara-Ricalde R. Complex location of a single rod contraceptive implant. Ginecol Obstet Mex 2014; 82 (10): 666-71.
- Gómez-Fredes PV, Pierucci A, Martín N, Urquiola C. Migración de implante anticonceptivo subdérmico a rama segmentaria de la arteria pulmonar. Revista Argentina de Radiología 2023; 86 (1). https://doi.org/10.24875/rar.m22000005
- Hindy JR, Souaid T, Larus CT, Glanville J, Aboujaoude R. Nexplanon migration into a subsegmental branch of the pulmonary artery: A case report and review of the literature: A case report and review of the literature. Medicine 2020; 99 (4): e18881. https://doi.org/10.1097/MD.0000000000018881
- Kafi Mallak F, Kopp Kallner H. Migration of a subdermal contraceptive implant into a subsegmental pulmonary artery and etonogestrel serum concentration over time - a case report. Eur J Contracept Reprod Health Care 2022; 27 (3): 261-64. https://doi.org/10.1080/13625187.2022.2036977
- Kew EP, Senanayake E, Djearaman M, Bishay E. Migration of contraceptive implant into the left pulmonary arterial system. Asian Cardiovasc Thorac Ann 2017; 25 (7-8): 537–539. https://doi.org/10.1177/0218492317716589
- Maybury EK, Affrin ZC, Popa C, Fowler M, et al. Nexplanonectomy-the surgical removal of an embolized implanted contraceptive device: a case report and review of the literature. J Med Case Rep 2024; 18 (1): 234. https://doi.org/10.1186/s13256-024-04547-7
- O’ Brien A, O’Reilly MK, Sugrue G, Lawler L, et al. Subdermal contraceptive implant embolism to a pulmonary artery. Ann Thorac Surg 2015; 99 (6): 2254-55. https://doi.org/10.1016/j.athoracsur.2014.12.017
- Park JU, Bae HS, Lee SM, Bae J, Park JW. Removal of a subdermal contraceptive implant (Implanon NXT) that migrated to the axilla by C-arm guidance: A case report and review of the literature. Medicine 2017; 96 (48): e8627. https://doi.org/10.1097/md.0000000000008627
- Patel A, Shetty D, Hollings N, Dodds N. Contraceptive implant embolism into the pulmonary artery. Ann Thorac Surg 2014; 97 (4): 14521452. https://doi.org/10.1016/j.athoracsur.2013.09.029
- Rivera F, Bianciotto A. Contraceptive subcutaneous device migration: what does an orthopaedic surgeon need to know? A case report and literature review. Acta Bio-Medica 2020; 91 (4-S): 232–237. https://doi.org/10.23750/abm.v91i4-S.9498
- Rowlands S, Mansour D, Walling M. Intravascular migration of contraceptive implants: two more cases. Contraception 2017; 95 (2): 211-14. https://doi.org/10.1016/j.contraception.2016.07.015
- Thomas PA, Di Stefano D, Couteau C, D’Journo XB. Contraceptive implant embolism into the pulmonary artery: Thoracoscopic retrieval. Ann Thorac Surg 2017; 103 (3): e271-e272. https://doi.org/10.1016/j.athoracsur.2016.08.094
- Moreira IF, Bianchini MP, Moreira GRC, Almeida AM, et al. Sexual function and metabolic/hormonal changes in women using long- term hormonal and non-hormonal contraceptives: a pilot study. BMC Women’s Health 2020; 20 (1). https://doi.org/10.1186/s12905- 020-01107-1