RESUMEN
ANTECEDENTES: La brucelosis es una de las enfermedades zoonóticas más frecuentes en la mayor parte del mundo. Mientras que en los países desarrollados han logrado con éxito su control, en los países en vías de desarrollo continúa siendo un gran problema de salud pública.
CASO CLÍNICO: Paciente primigesta, con embarazo múltiple bicorial biamniótico. En el tercer trimestre de la gestación inició con dolor en la articulación sacroiliaca derecha y fiebre intermitente durante el puerperio. Ante la persistencia de la fiebre de origen desconocido durante el puerperio inmediato, se le practicaron múltiples pruebas serológicas para gérmenes típicos y atípicos; se diagnosticó brucelosis. Recibió tratamiento con doxiciclina, con lo que desapareció el cuadro clínico.
CONCLUSIÓN: La infección por Brucella se asocia con morbilidad obstétrica y neonatal y se diagnostica con el aislamiento microbiológico o aumento de los títulos de anticuerpos. El inicio oportuno del tratamiento con rifampicina asociado con trimetoprima-sulfametoxazol disminuye la morbilidad y mortalidad materna y perinatal.
PALABRAS CLAVE: Brucelosis, bacilo, embarazo, articulación sacroilíaca
ABSTRACT
BACKGROUND: Brucellosis is a bacterial infection caused by a gram-negative bacillus that primarily affects people in developing countries. It is associated with contact with infected animals or consumption of unpasteurized milk products. Maternal infection is rare without maternal-fetal morbidity.
CLINICAL CASE: A patient in her first pregnancy with a biamniotic bicoronal multiple pregnancy. In the third trimester of pregnancy, she developed pain in the right sacroiliac joint and intermittent fever during the puerperium. Given the persistence of fever of unknown origin in the immediate postpartum period, multiple serologic tests for typical and atypical pathogens were performed; brucellosis was diagnosed. She was treated with doxycycline and the clinical symptoms disappeared.
KEYWORDS: Brucellosis, Bacillus, Pregnancy, Sacroiliac joint, Rifampin
ANTECEDENTES
La brucelosis humana, o fiebre ondulante, es una zoonosis causada por la bacteria Brucella. Es una infección frecuente en todo el mundo y un problema de salud pública en países en vías de desarrollo. Es más prevalente en el oriente medio, zona mediterránea, África subsahariana y algunos países de América del Sur y Asia.1,2 En el mundo se reportan, aproximadamente, medio millón de nuevos casos anuales.1-4 La incidencia varía de 0.03 a 160 casos por cada 100,000 habitantes. En los países industrializados está prácticamente erradicada.3
Brucella es un bacilo gramnegativo, aerobio estricto, inmóvil, no encapsulado ni esporulado. Existen cuatro especies patógenas para los humanos: B. abortus, B. melitensis, B. suis y B. canis. La más invasiva y patógena es B. melitensis.3,4
La trasmisión ocurre por el contacto directo con animales infectados: cabras, ovejas, vacas, cerdos o perros a través de sus secreciones o aerosoles inhalados. El consumo de alimentos contaminados como carnes o productos lácteos no pasteurizados es la forma más frecuente de infección.1-4 En menor proporción se ha documentado la trasmisión de persona a persona a través del contacto sexual, lactancia materna, trasfusión sanguínea, trasplantes y exposición perinatal.4
La presentación clínica es variada, puede afectar cualquier sistema y cursar asintomática hasta la muerte.3 El cuadro clínico más grave es en pacientes con inmunosupresión, que son los de mayor tasa de morbilidad y mortalidad.5
La brucelosis es infrecuente en las embarazadas. Este conocimiento está fundamentado en estudios observacionales, reportes y series de casos; de ahí que no se disponga de datos significativos referentes a las características de la infección, gravedad y desenlaces obstétricos.1,5,6 La seroprevalencia varía entre las diferentes regiones, desde el 1% al 12.2%.1,2,6 La incidencia acumulada es de 0.42 a 3.3 por cada 1000 pacientes obstétricas.2 Las mujeres embarazadas, con factores de riesgo (ingesta de productos lácteos no pasteurizados, contacto estrecho con animales infectados, antecedente de abortos recurrentes, vivienda en zonas rurales con bajos ingresos socioeconómicos) suelen tener mayor seropositividad6,7 que se asocia con desenlaces obstétricos adversos: aborto, infecciones intraamnióticas y complicaciones sistémicas maternas.3,5
Hay un aumento del riesgo de aborto espontáneo del 43% durante el primer y segundo trimestre del embarazo.8 Así mismo, el riesgo de parto pretérmino es del 13.9%, comparado con la población general del 11%, muerte fetal de 8.1%, secuelas en neonatos con brucelosis congénita del 2% y corioamnionitis.9
Está demostrado que conforme mayor sea la seroprevalencia durante el embarazo, mayor es el riesgo de complicaciones. Las tasas de complicaciones disminuyen si el tratamiento con aminoglucósidos se inicia en el trascurso de las dos semanas posteriores a la aparición de los síntomas.10
Existen diferentes teorías que explican la fisiopatología de la brucelosis en el embarazo. Está demostrado que esta bacteria puede infectar y afectar diferentes tipos de células trofoblásticas, alterar la función de producción de hormonas que impiden la habilidad del citotrofoblasto a convertirse en sincitiotrofoblasto y alterar la capacidad de invasión de los trofoblastos extravellosos.11 Se cree que esta infección produce una severa inflamacion en la placenta mientras se replica, generada por el aumento del factor de necrosis tumoral alfa, lo que lleva al aborto.12 Por último, entre las teorías se considera que la brucelosis genera que las células inmunitarias: macrófagos, neutrófilos y monocitos produzcan citocinas proinflamatorias (IL-8, IL-6 y MCP-1) que incrementan la inflamación en el trofoblasto y favorecen las complicaciones en el embarazo.13
CASO CLÍNICO
Paciente primigesta de 19 años, procedente del área rural de Yopal, Casanare, con embarazo gemelar bicorial biamniótico de 32 semanas. Ingresó al Hospital de la Samaritana de Bogotá debido a un cuadro clínico de un mes de evolución de dolor lumbosacro paravertebral derecho, intermitente, tipo picada, de intensidad 5-10, limitación de la marcha y percepción de actividad uterina irregular de dos días. Antecedente laboral: trato con ganado bovino. En la auscultación inicial los signos vitales se encontraron en normalidad. El útero: grávido, con dos fetos vivos longitudinales, uno de los gemelos en presentación pélvica. Dilatación del cuello uterino de tres centímetros, con borramiento del 80%.
Al examen osteomuscular se advirtió dolor en la región paravertebral lumbosacra y en la articulación sacroiliaca derecha, sin déficit motor ni sensitivo en los miembros inferiores, signos de Lasègue negativos.
En la ecografía obstétrica se evidenció la biometría concordante con las semanas de gestación de ambos fetos; uno de ellos con anhidramnios agudo, con bolsillo vertical de 5 mm. Ante el diagnóstico de trabajo de parto pretérmino y primer feto en presentación podálica se decidió la cesárea, que transcurrió sin complicaciones, con recién nacido (1) con ausencia de líquido amniótico, peso 1575 g, Apgar 8-9 y el otro recién nacido (2) con escaso líquido amniótico, meconio espeso, peso de 1645 g, Apgar 7-8. Ambos tuvieron síndrome de dificultad respiratoria que requirió hospitalización, administración de surfactante pulmonar y ventilación mecánica no invasiva. Durante la hospitalización ninguno mostró signos de infección por lo que se dieron de alta del hospital a los 46 días, sin alteración en el neurodesarrollo.
Al primer día de posoperatorio la paciente experimentó intensificación del dolor en la articulación sacroilíaca derecha, de intensidad 8-10 con limitación a la bipedestación por el dolor. En la valoración del neurocirujano se evidenciaron el dolor a la palpación de la articulación sacroilíaca derecha y la limitación para los arcos de movimiento, secundaria al dolor incapacitante; signo de Patrick derecho positivo. Se estableció el diagnóstico de sacroileítis. Se trató con analgesia multimodal, sin mejoría, por lo que se procedió al bloqueo epidural sacroiliaco, guiado por ecografía, sin complicaciones.
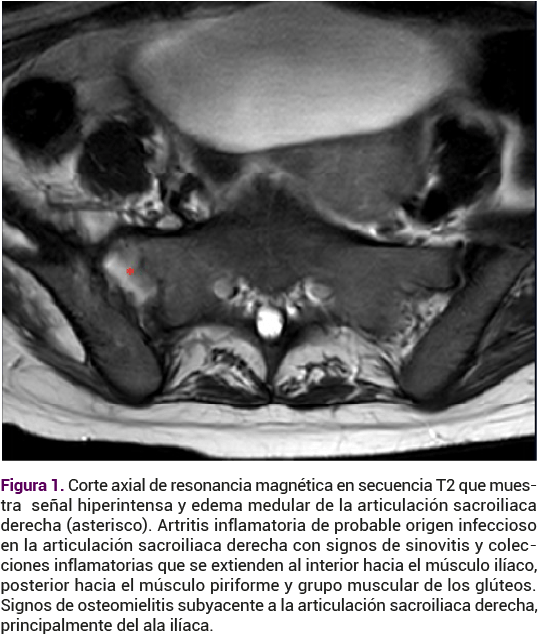
Ante la persistencia del dolor, al décimo día de hospitalización se practicó un estudio de resonancia magnética de la articulación sacroiliaca derecha, con hallazgos en relación con la sacroileítis aguda derecha extensa (Figura 1).
Se le indicó tratamiento con vancomicina y clindamicina. Al duodécimo día se le hizo un lavado, desbridamiento y secuestrectomía de los huesos pélvicos, de la articulación sacroiliaca y del sacro. En el procedimiento se documentó que la articulación sacroiliaca se encontró móvil, con fibrosis, el ligamento sacroiliaco anterior con membranas fibrinoides y a la altura del sacro una membrana fibrinoide, sin material purulento. Se tomaron cultivos del periostio iliaco derecho, ligamento sacroiliaco anterolateral, sacro y sacroiliaco que se reportaron negativos para gérmenes comunes y micobacterias.
A partir del decimoséptimo día de hospitalización la paciente comenzó a tener picos febriles diarios, vespertinos. Por ello se escaló el tratamiento antibiótico a cefepime, se continuó la vancomicina y se adicionó metronidazol. Se practicó un nuevo lavado quirúrgico en búsqueda de colección o de evidencia de la causa de persistencia de la fiebre. En el lavado no se evidenciaron signos de infección en la articulación sacroiliaca. Los análisis paraclínicos reportaron: leucopenia de 2280 cel/mL, neutropenia de 1750 cel/mL, linfopenia 380 cel/mL, plaquetas 276,000 cel/mL , función hepática y renal normal, hemocultivos negativos, urocultivo negativo, ecografía pélvica con útero puerperal y el endometrio y la histerorrafia en situación de normalidad. El ecocardiograma transtorácico también se informó en normalidad, sin signos de endocarditis.
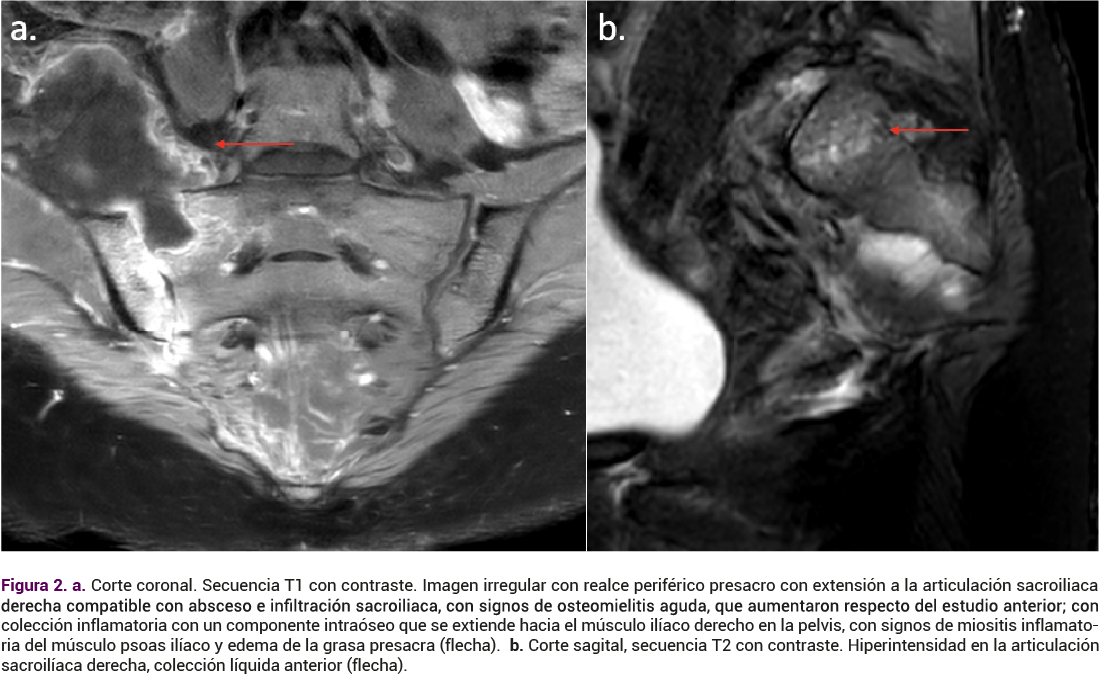
Debido a la persistencia de los picos febriles se tomó un control por resonancia magnética de la articulación sacroiliaca que documentó la persistencia de extensos signos de sacroileítis aguda derecha (Figura 2). Debido a la ausencia macroscópica de infección en el lavado, se inició el estudio de enfermedades que causan sacroileitis atípicas. Entre estas se solicitó el de enfermedades vectoriales, que se reportaron negativas e IgM para Brucella con resultado positivo, no se contó con IgG. De inmediato se inició el tratamiento con rifampicina; sin embargo, debido al desabastecimiento del medicamento se cambió a doxiciclina, vía oral, 100 mg cada 12 horas para completar seis semanas. La evolución fue favorable, con modulación de la respuesta inflamatoria sistémica, sin nuevos picos febriles, con alta del hospital al vigésimo quinto día de puerperio, con analgésico no esteroideo y terapia física. En el seguimiento la paciente se desplazó a su ciudad de origen, completó el tratamiento antibiótico con desaparición completa de los síntomas y a los 24 meses permanece asintomática, sin limitación para la marcha, con desaparición completa del cuadro clínico.
DISCUSIÓN
Clínica
La clínica de la brucelosis tiene variaciones importantes, afecta cualquier sistema del organismo y se clasifica clínicamente en seis tipos3,4.
• Subclínica: asintomática, la infección se documenta por serología positiva.
• Aguda: posterior a un periodo de incubación de semanas o meses, como una enfermedad leve, transitoria o grave dependiendo de la cepa infectante4. Los síntomas son inespecíficos: astenia, adinamia, escalofríos, mialgias, artralgia, lumbalgia e hiporexia. Del 80 al 90% de los casos tienen fiebre, que se denomina fiebre ondulante o intermitente por su patrón característico en el que los picos ocurren en horas de la tarde3,4,5.
• Subaguda: manifestaciones clínicas entre los 3 a 12 meses del diagnóstico.
• Localizada: complicación focal tipo: espondilitis, osteomielitis, sacroileitis o abscesos.
• Crónica: manifestaciones clínicas durante más de un año posterior al diagnóstico. Se manifiesta sin fiebre5; casi siempre secundaria a un tratamiento inadecuado o una enfermedad focal no diagnosticada4.
• Recidivante: nueva infección posterior al tratamiento. Las tasas de recidiva son del 5 al 15% de los casos en los seis meses posteriores al tratamiento de forma menos grave, secundaria al mal apego al tratamiento3; sin embargo, también puede ser posterior a un tratamiento antibiótico inadecuado por mecanismos de resistencia intracelular de la Brucella4.
La infección durante el embarazo puede afectar más de un órgano. El 50% de los casos afecta el sistema osteoarticular y provoca: sacroileítis, artritis periférica y espondilodiscitis; sobre todo, daña las vértebras lumbares y las articulaciones: tobillos, rodillas y caderas. Con menos frecuencia afecta los sistemas nervioso central (10%), urinario (10%) y cardiovascular. Las infecciones que más ponen en riesgo de muerte son la hepatobiliar, respiratorias y dermatológicas3,4.
La brucelosis se asocia con desenlaces obstétricos adversos en un 30 a 50% de los casos. Es causa de: abortos, infección intraamniótica, parto pretérmino, bajo peso al nacer, infección congénita, muerte fetal y morbilidad neonatal como neumonía aspirativa o meningitis3-6. Las tasas de abortos espontáneos por brucelosis varían del 24 al 53%6,14,15,16 y las tasas de parto pretérmino del 7 al 295; complicación que pudo estar asociada en la paciente del caso; sin embargo, el embarazo gemelar pudo ser suficiente para desencadenar el trabajo de parto pretérmino. Una limitación que se tuvo fue que no se pudo descartar una infección intramniótica.
Diagnóstico
La brucelosis debe sospecharse en pacientes con síntomas inespecíficos, factores de riesgo y fiebre de origen desconocido3. Los hallazgos de laboratorio pueden incluir: anemia, leucopenia, neutropenia, trombocitopenia, pancitopenia o leucocitosis con linfocitosis3,4. La inmunidad celular es decisiva: los anticuerpos de la inmunoglobulina M (IgM) aumentan en la primera semana y los de la inmunoglobulina G (IgG) a partir de la segunda semana. Posterior a cuatro semanas de tratamiento completo y efectivo disminuyen sus concentraciones. La IgM puede permanecer positiva durante meses o años a títulos bajos; sin embargo, una concentración elevada de anticuerpos IgG o IgM de seis meses o más implica una infección crónica o recidiva3. Otra limitación del caso fue que ya no se obtuvo una nueva determinación de IgM e IgG seis meses después del cuadro.
La confirmación de la infección debe hacerse con estudios microbiológicos de líquidos o tejidos corporales con cultivos (sangre, orina, líquido cefalorraquídeo, líquido sinovial, líquido pleural o biopsias), con variación de su sensibilidad según la muestra y medio de cultivo utilizado3,4. Los hemocultivos se reportan positivos en 10 al 30% de los casos y si hay infección por B. melitensis pueden alcanzar una positividad hasta del 85%; en la paciente del caso resultó negativo. El cultivo de médula ósea es el patrón de referencia. Su crecimiento es lento, más sensible que el hemocultivo, pero más invasivo y en pacientes con enfermedad crónica hay una menor probabilidad de crecimiento17.
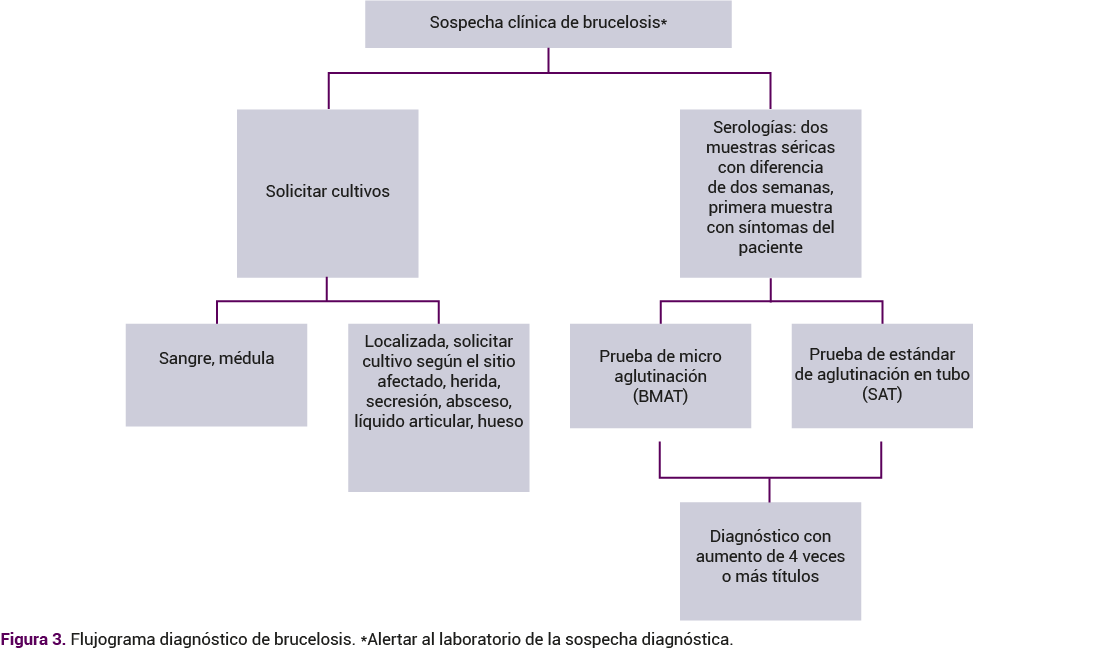
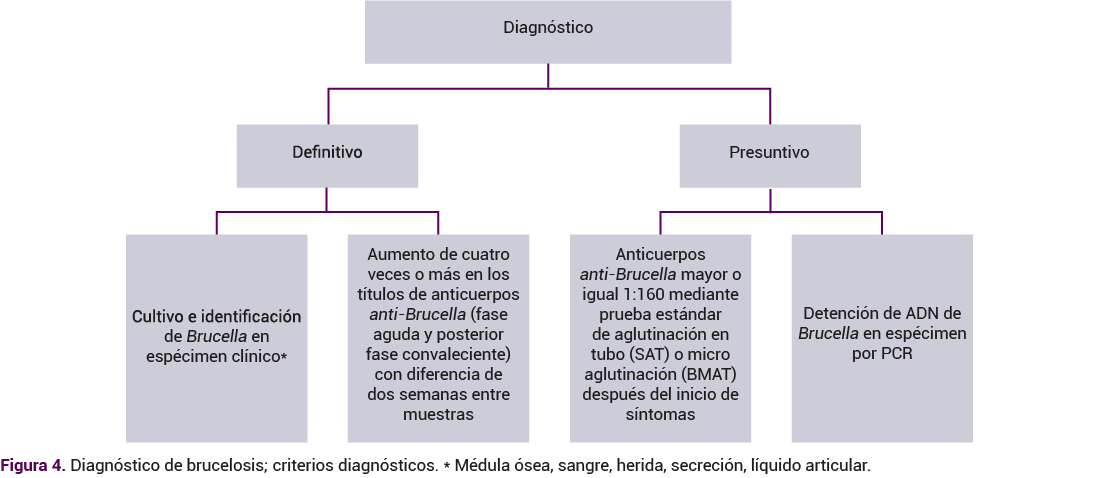
Si no se dispone de la confirmación microbiológica, en el contexto de sospecha clínica, se recurre a la serología como prueba de aglutinación en tubo estándar (SAT) que detecta anticuerpos contra B. suis, B. abortus y B. melitensis. Los resultados son significativos, considerando una sospecha diagnóstica con títulos positivos 1:160 en zonas endémicas y 1:80 en zonas no endémicas4. El diagnóstico se confirma si hay cuadruplicación o más del título de anticuerpos en muestras de suero de la fase aguda y convalecencia que se obtienen con dos semanas de diferencia4,17. Figuras 3 y 4
La paciente del caso tenía factores de riesgo, clínica y laboratorios compatibles, y desaparición del cuadro clínico luego de haber iniciado el tratamiento médico dirigido; sin embargo, no se contó con cultivo positivo, ni reporte de incremento en la titulación, por lo que no pudo confirmarse el diagnóstico definitivo. Lo más relevante del caso fue el desafío diagnóstico, pues los síntomas principales se dieron durante el puerperio, cuando se descartaron varios diagnósticos más comunes y, posteriormente, gérmenes atípicos, como Brucella spp.
En Colombia se reportó el primer caso de brucelosis materna en el 2020, que también cursó con parto pretérmino a las 33 semanas, síntomas inespecíficos de dolor pélvico y fiebre, con hemocultivos para Brucella spp positivos. El diagnóstico se confirmó retrospectivamente. Llama la atención que también cursó con complicación musculoesquelética a los cuatro meses de haber completado el tratamiento, teniendo en cuenta la probabilidad de recaída de hasta el 11%18,19.
Se han reportado, aproximadamente, 500 casos de brucelosis en embarazadas confirmados por seroaglutinación, con manifestaciones inespecíficas. Las principales son: fiebre, dolor articular y artralgia. Estas cursaron en un 37% con parto pretérmino, sin reportar complicaciones de sacroileítis20. Existen solo dos casos de sacroileítis por brucelosis reportados en la bibliografía, en los que el diagnóstico también fue tardío durante el puerperio, teniendo en cuenta la inespecificidad de la clínica21.
Prevención
No existe vacuna para prevenir la infección por Brucella en humanos. Las medidas de prevención son4,17:
• Tratamiento de productos lácteos, evitar el consumo de lácteos no pasteurizados y de carnes crudas. • Protocolos de protección para trabajadores con riesgo de exposición ocupacional en mataderos, trabajadores agrícolas, veterinarios, trabajadores de laboratorios que manipulan tejidos de animales. • Precauciones para prevenir la trasmisión de persona a persona: evitar las relaciones sexuales y la lactancia materna hasta completar el tratamiento; evaluación clínica y serológica de personas que conviven con pacientes con diagnóstico de brucelosis.
Tratamiento
El objetivo del tratamiento con antibiótico en la paciente embarazada tiene el propósito de disminuir las complicaciones obstétricas asociadas1,2,5. No hay ensayos clínicos que hayan investigado cuál es el mejor antibiótico durante el embarazo. Las recomendaciones se basan en estudios observacionales. La Organización Mundial de la Salud recomienda la rifampicina como primera línea de tratamiento durante el embarazo, asociada con otro antibiótico con efecto bactericida para disminuir la recurrencia: trimetoprima-sulfametoxazol u otras alternativas de segunda línea como eritromicina o ceftriaxona5,17,22,23.
El esquema de tratamiento con rifampicina y trimetoprima-sulfametoxazol se administra durante seis semanas, sobre todo a pacientes con diagnóstico temprano (Cuadro 1)5,8,17,24. Posterior a las 36 semanas se suspende la trimetoprima-sulfametoxazol por el riesgo de ictericia y kernícterus neonatal2,3.

En series de casos de pacientes embarazadas, los aminoglucósidos también se han indicado asociados con rifampicina, sin evidenciar ototoxicidad fetal5. La formulación de tetraciclinas está contraindicada en las embarazadas pero puede indicarse para el tratamiento posterior al parto; desde luego suspendiendo la lactancia hasta después de concluir el tratamiento. Los casos de reinfección o cronicidad de brucelosis son infrecuentes debido a la inmunidad adquirida posterior a la infección4.
En las pacientes con brucelosis localizada se indica tratamiento antibiótico prolongado con adición de betalactámicos, como ceftriaxona, con intervenciones quirúrgicas para el drenaje del foco infeccioso4.
En el caso aquí reportado se indicó tetraciclina en virtud del diagnóstico en el puerperio y sin disponibilidad de rifampicina, junto con drenaje quirúrgico y terapia física, con remisión total de la enfermedad.
CONCLUSIÓN
La infección por Brucella es una enfermedad de baja frecuencia y, quizá por ello subdiagnosticada. Su mayor repercusión en personas inmunosuprimidas, como las embarazadas; se asocia con morbilidad obstétrica. Se diagnostica con el aislamiento microbiológico o aumento de los títulos de anticuerpos. El inicio oportuno del tratamiento disminuye la morbilidad y mortalidad materna y perinatal. La paciente del caso clínico experimentó una evolución poco común, circunstancia que dificultó el diagnóstico; aún así, tuvo la complicación más frecuente asociada con la infección por brucela en población joven: sacroileítis.
REFERENCIAS
- Bosilkovski M, Arapović J, Keramat F. Human brucellosis in pregnancy - an overview. Bosn J Basic Med Sci 2020; 20 (4): 415-22. https://doi.org/10.17305/bjbms.2019.4499
- Majzoobi MM, Teimori R, Nouri S, Karami M, Bosilkovski M, Saadatmand A. Maternal, fetal, and neonatal outcomes of gestation in women with and without Brucella infection. J Res Health Sci 2023; 23 (1): e00575. https://doi.org/10.34172/jrhs.2023.110
- Gul HC, Erdem H. Brucelosis (species de Brucella). In: Bennett J, Dolin R, Blaser M, eds. Mandell, Douglas, and Bennett’s Principles and Practice of Infectious Diseases. 9 ed. Mdrid: Elsevier, 2021; 2753-58.
- Salvana E, Salata R. Brucelosis. En: Goldman L, Schafer A, eds Goldman - Cecil Tratado de Medicina Interna. 23 ed. Madrid: Elsevier, 2021; 1951-53.
- Vilchez G, Espinoza M, D’Onadio G, Saona P, Gotuzzo E. Brucellosis in pregnancy: clinical aspects and obstetric outcomes. Int J Infect Dis 2015; 38: 95-100. https://doi.org/10.1016/j.ijid.2015.06.027
- Shrivastava A, Sangale A. Brucellosis in pregnancy. J Obstet Gynecol India 2000; 50 (4): 14-6.
- Khan MY, Mah MW, Memish ZA. Brucellosis in pregnant women. Clin Infect Dis 2001; 32 (8): 1172-7. https://doi.org/10.1086/319758
- Johari S, et al. Management and outcomes of pregnancy complicated by brucellosis. Arch Gynecol Obstet 2016; 294: 605-14. https://doi.org/10.1007/s00404-016-4090-8
- Roushan MR, Baiani M, et al. Clinical and laboratory findings, treatment and outcome of brucellosis in pregnancy: a retrospective study. BMC Infect Dis 2019; 19: 734. https://doi.org/10.1186/s12879-019-4347-7
- Khan MY, et al. Brucellosis in pregnancy. Clin Infect Dis 2001; 32 (8): 1172-7. https://doi.org/10.1086/319758
- Allard M, et al. Brucella infection in human trophoblast. Placenta 2019; 83: 1-9. https://doi.org/10.1016/j.placenta.2019.06.393
- Fioravanti A, et al. Brucella abortus induces placental inflammation in pregnant mice. Infect Immun 2019; 87 (8): e00111-19. https://doi.org/10.1128/IAI.00111-19
- Carvalho N, et al. Brucella abortus infection and cytokine response in trophoblast cells. Microbes Infect 2017; 19: 392-401. https://doi.org/10.1016/j.micinf.2017.04.005
- Gulsun S, et al. Brucellosis in pregnancy. Trop Doct 2011; 41 (2): 82-4. https://doi.org/10.1258/td.2010.100340
- Gur A, et al. Brucellosis in pregnancy: a case series. J Infect Dev Ctries 2019; 13 (9): 838-42. https://doi.org/10.3855/jidc.11520
- Roushan MR, et al. Brucellosis in pregnancy: results of a study of 10 cases. Int J Infect Dis 2002; 6 (3): 208-10. https://doi.org/10.1016/S1201-9712(02)90133-6
- Corbel MJ. Brucellosis in humans and animals. Geneva: WHO, 2006.
- Velásquez C, et al. Brucelosis durante el embarazo: reporte de caso. Rev Colomb Obstet Ginecol 2020; 71 (3): 275-83. https://doi.org/10.18597/rcog.3537
- Al-Tawfiq JA. Brucellosis and human health. Curr Opin Infect Dis 2022; 35 (5): 415-20. https://doi.org/10.1097/QCO.0000000000000884
- Al-Shamahy HA, et al. Brucellosis in pregnancy. Trop Doct 2000; 30 (1): 23-5. https://doi.org/10.1177/004947550003000110
- Tugrul S, et al. Sacroiliitis due to brucellosis during pregnancy: a case report. Arch Gynecol Obstet 2006; 274: 353-5. https://doi.org/10.1007/s00404-006-0174-4
- WHO. Brucellosis in humans and animals. WHO/CDS/EPR/2006.7.
- Ramos JM, et al. Brucellosis. Clin Microbiol Infect 2017; 23 (9): 646-52. https://doi.org/10.1016/j.cmi.2017.02.013
- Ariza J, Bosilkovski M, Cascio A, et al. Perspectives for the treatment of brucellosis in the 21st century: the Ioannina recommendations. PLoS Med 2007; 4 (12): e317. https://doi.org/10.1371/journal.pmed.0040317